Introducción
Las levaduras del género Hanseniaspora son las más frecuentemente aisladas en uvas y otras frutas, es habitual que esta especie aparezca al inicio de las fermentaciones espontáneas y después van siendo desplazadas generalmente por Saccharomyces (Romano et al. 2003, Medina et al. 2013, Lleixa et al. 2016). Existen 23 especies de Hanseniaspora, de ellas diez se han encontrado asociadas a uvas y vino, dentro de las cuales hay unas muy poco fermentadoras, definidas como de las frutas, y otras como fermentadoras (Valera et al. 2021).
En el grupo de las frutas encontramos Hanseniaspora valbyensis, Hanseniaspora guilliermondii, Hanseniaspora uvarum, Hanseniaspora opuntiae, Hanseniaspora thailandica, Hanseniaspora meyeri, y Hanseniaspora clermontiae que presenta una evolución caracterizada como rápida debido a su variabilidad genética muy inestable. En el grupo de las fermentadoras se encuentran, Hanseniaspora vineae, Hanseniaspora osmophila, y Hanseniaspora occidentalis que presentan evolución lenta en su genoma debido a su mayor estabilidad genética (Steenwyk et al., 2019). Estas diferencias genéticas tienen también una representación fenotípica, respecto a la capacidad fermentativa y la producción de aromas (Valera et al., 2021; Martin et al., 2018).
Durante décadas se consideró este género de levaduras como un grupo de microorganismos no deseados para llevar a cabo la fermentación. Especialmente por ser consideradas causantes de aumentar la acidez volátil (Ciani and Picciotti, 1995), aunque esta característica es dependiente de la cepa, hay especies que han sido habitualmente caracterizadas como productoras de ácido acético, especialmente las del grupo de la fruta. Sin embargo, cabe destacar como ejemplo, que algunas cepas de Hanseniaspora vineae han mostrado una producción de acidez volátil similar o menor a la observada en Saccharomyces cerevisiae en las mismas condiciones de fermentación (Del Fresno et al., 2021, Medina et al., 2013).
Por otra parte, la capacidad fermentativa de Hanseniaspora es moderada, por ello lo más habitual es usar cultivos mixtos. Sin embargo, el potencial aromático de algunas cepas de Hanseniaspora está empezando a ser explotado por los enólogos para contribuir a una mayor diversidad aromática en los vinos finales con estrategias de co-inoculación con Saccharomyces en baja proporción (10-20% del inoculo inicial) (Gallo et al. 2024). El uso de cultivos mixtos de Hanseniaspora y Saccharomyces además de mejorar el perfil aromático ofrece diversos beneficios. Entre ellos, la disminución del contenido alcohólico, modular la producción de ácidos y aumentar la cantidad de antocianos. Además, debido a la capacidad proteolítica de algunas cepas, puede disminuir la turbidez en vinos (Martin et al. 2018, van Wyk et al. 2023, Carrau et al. 2023).
La forma en que las levaduras contribuyen a la formación de aromas durante el proceso fermentativo es variada. Por una parte, el uso de los aminoácidos a través de diversas rutas metabólicas para producir alcoholes superiores y sus correspondientes acetatos (Fig. 1), que en Hanseniaspora está desarrollado por el gran número de copias de genes que participan de esta vía.
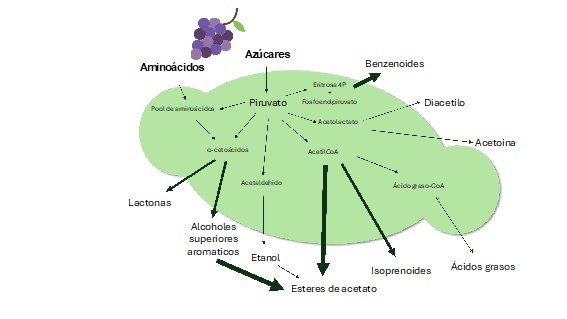
En Hanseniaspora también se ha identificado la alta producción de bencenoides e isoprenoides en comparación con Saccharomyces, que tienen impacto sensorial en el producto final (Martin et al. 2016; Martin et al. 2022). Algunos sesquiterpenos se destacan con mayor producción en Hanseniaspora que en Saccharomyces (Martin et al. 2022), y entre los monoterpenos se ha detectado una producción interesante de safranal en H. vineae, que estaría en concentraciones superiores a su umbral sensorial (Del Fresno et al. 2022). Otros procesos que contribuyen al aroma final del vino es la producción de β-glucosidasa extracelular que permite la liberación de precursores aromáticos ligados a azúcares presentes en las uvas, y la lisis celular que libera compuestos relacionados con los aromas y la textura del vino. En esta revisión profundizaremos en los compuestos derivados de aminoácidos aromáticos, la producción de enzimas glucosidasas y lisis celular.
Producción de ésteres de acetatos y alcoholes superiores a partir de aminoácidos aromáticos
El perfil aromático de los vinos producidos con cultivos mixtos de Hanseniaspora y Saccharomyces varía sensiblemente respecto a los vinos elaborados con cultivos puros de Saccharomyces. Esta modulación debida a la interacción de ambas cepas se puede apreciar en el conjunto de los aromas, pero en la mayoría de las fermentaciones lo que se observa más claramente es un aumento significativo de los ésteres de acetato de los alcoholes superiores. Especialmente aquellos producidos a partir de los alcoholes superiores que derivan de aminoácidos aromáticos (feniletanol, triptofol y tirosol). Esta capacidad de acetilación resulta interesante debido a que los acetatos de ésteres de alcoholes superiores tienen un umbral de percepción sensorial más bajo que los correspondientes alcoholes (Martin et al., 2018).
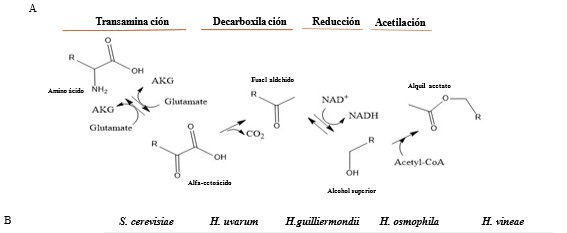
La producción de ésteres a partir de un acetato y un alcohol se lleva a cabo en cuatro reacciones consecutivas (Fig. 2A). En primer lugar, una transaminación de los aminoácidos donde participarían homólogos de los genes BAT1, ARO8 y ARO9 (Fig 2B) de S. cerevisiae.
|
Las especies del género Hanseniaspora que han sido analizadas no presentan homólogos del gen BAT2 que participaría en la transaminación en S. cerevisiae, pero sí tienen varias copias más de los genes ARO que Saccharomyces. Después, los α-cetoácidos resultantes se descarboxilan por acción de los productos de genes como PDC1 y ARO10, dando lugar a los correspondientes aldehídos. Éstos producen alcoholes superiores mediante alcohol deshidrogenasas como las codificadas por ADH6. Estas tres reacciones corresponden al mecanismo de Ehrlich y culminan con la producción de alcoholes superiores. Finalmente, éstos se pueden transformar en ésteres de acetatos mediante la actividad de acetiltransferasas como las codificadas por alcohol acetil transferasas (AAT) que condensan los alcoholes con el grupo carboxílico de la acetil coenzima A. Se conoce que algunas cepas del género Hanseniaspora tienen gran número de copias de genes candidatos relacionados con la acetilación, lo que podría explicar la alta tasa de acetilación de alcoholes superiores que se detecta en el medio extracelular en fermentaciones llevadas a cabo con especies de este género.
ATF1 y ATF2 sintetizan la producción de ésteres volátiles en S. cerevisiae (Verstrepen et al., 2003). En el caso de H. osmophila y H. vineae, presentan ATF2, pero no ATF1 y H. uvarum no presenta homólogos de ninguna de ellas (Valera et al., 2021). Sin embargo, hay algunos aminoácidos conservados en las secuencias con homología a ATF2 y una proteína hipotética (GenBank accession number OEJ85955.1), sin homología con S. cerevisiae que presentan dominio AATasa. Recientemente han sido publicadas las primeras herramientas eficientes para modificar genes en H. uvarum (Badura et al., 2021; Heinisch et al., 2023). En estos ensayos se llegó a construir un mutante de H. uvarum sin las dos copias de AATasas que presentó una producción de ésteres de acetato mucho menor que la cepa parental (Badura et al., 2021).
Se ha visto que también los productos del gen homólogo a SLI1 podrían realizar este paso en Hanseniaspora vineae (Giorello et al. 2019, Valera et al. 2021). En H. vineae, las copias de los genes SLI1 se localizan en tándem dentro del genoma. Cada una de ellas presenta homología con una AATasa de H. osmophila. Sin embargo, las AATasas de H. uvarum se salen de ese clúster.
H. guillermondii UTAD222 tiene 4 genes que codifican AAT y que se expresan diferencialmente a lo largo de la fermentación. Además, según Seixas et al. 2023, esta expresión está modulada por el balance de carbono-nitrógeno en el medio, resultando que menor proporción de carbono respecto a nitrógeno aumenta la actividad acetil transferasa en el medio, generando más acetatos, concretamente más acetato de isoamilo (aroma frutal, banana) y acetato de β-feniletilo (miel, floral).
En S. cerevisiae hay dos regiones esenciales para los genes ATF. El primero es el motivo WRLICLP, el cual no está estrictamente conservado en microorganismos (van Laere et al., 2008). El segundo es el motivo catalítico H-X-X-X-D que aparece en AATsas vegetales. Los residuos catalíticos His y Asp se ha visto que son cruciales para la función AATasa y forman parte del sitio activo en estas enzimas (D’Auria 2006, Beekwilder et al., 2004).
Actividad β-glucosidasa
La mayor parte de los precursores aromáticos de la uva están ligados a azúcares, por esa razón no son perceptibles a través del olfato. Para poder ser percibidos y formar parte del aroma del vino, los compuestos aromáticos tienen que ser liberados para que sean volátiles. En uvas, dos compuestos volátiles importantes que se encuentran ligados son los alcoholes bencílico y β-feniletílico que, según el proceso de fermentación utilizado, se liberan en menor o mayor proporción (Versini et al. 1999). La actividad enzimática que participa en este proceso de liberación es la β-glucosidasa que rompe enlaces glucosídicos. Esta actividad está presente en las uvas y también en algunos microorganismos, pero se encuentra inhibida por azúcares. La actividad β-glucosidasa se puede dar avanzada la fermentación. Por ello la selección de levaduras que tengan esta actividad puede ser de interés para liberar aromas varietales en el proceso de vinificación (Zhang et al., 2021).
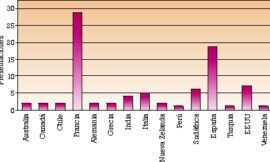
No es común que las levaduras Saccharomyces tengan esta actividad, sin embargo, las especies del género Hanseniaspora pueden crecer en celobiosa como única fuente de carbono, lo que demuestra que tienen actividad β-glucosidasa (van Wyk et al., 2023). Perez et al. en 2011 vieron diferencias en la intensidad de actividad β-glucosidasa en 3 cepas de H. vineae y 3 cepas de H. uvarum de forma semicuantitativa. Más recientemente, en un estudio realizado con 26 cepas diferentes de H. uvarum se vio que presentaban distintos niveles de actividad β-glucosidasa analizando aromas liberados por esta enzima por cromatografía (Guaragnella et al. 2020).
Realizando una comparación in silico de diferentes secuencias de posibles β-glucosidasas en los genomas de Hanseniaspora vemos que se presentan diferencias entre ellas. Atendiendo a la predicción de secuencia de aminoácidos de las distintas actividades β-glucosidasa, es evidente que se pueden relacionar las secuencias de las especies de Hanseniaspora que corresponden al grupo del vino y al grupo de la fruta. Existen tres tipos de β-glucosidasa atendiendo a la clasificación filogenética de sus secuencias (Fig. 3).
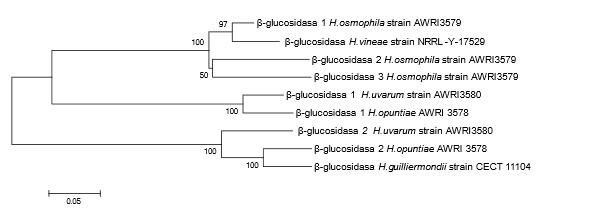
Y algunas cepas pueden presentar varias actividades con distinta secuencia en su genoma. Este es el caso de H. osmophila AWRI3579 que tiene tres homólogos de β-glucosidasa, uno parecido a la única encontrada en H. vineae y otros dos diferentes.
Lisis celular
En el caso particular de la especie H. vineae se ha comprobado que varias cepas presentan una detención en el ciclo celular. Esta parada no se observó en otras especies del género como H. uvarum, H. opuntiae o H. osmophila y tampoco en Saccharomyces (Schwarz et al 2022). H. osmophila, H. opuntiae y H. uvarum, muestran un comportamiento similar a S. cerevisiae. Según lo esperable, hay una gran proporción de células en fase G2/M en las fases de crecimiento rápido o exponencial, pero a medida que llegan a la fase estacionaria, la mayoría de las células se encuentran en un estado de quiescencia en fase G0. H. vineae, por el contrario, detiene su ciclo celular en G2/M en la fase estacionaria. La explicación parece ser una respuesta a la alta concentración de nitrógeno (Schwarz et al. 2023). Para elucidar esta diferencia en el comportamiento de la especie H. vineae se buscaron genes que pudieran variar entre H. osmophila y H. vineae, ambas pertenecientes al clado de evolución lenta. Se encontraron 38 genes ausentes en H. vineae en comparación con H. osmophila. De entre estos genes, es especialmente interesante ATG5 que codifica una proteína conservada relacionada con la respuesta autofágica y las dianas de la vía citoplasma-vacuola. Este gen también se ha relacionado con la vía de la diana de rapamicina (TOR) y la entrada en estado de quiescencia. Su producto, ATG5p pertenece a la ruta de autofagia en las levaduras donde es parte de un complejo citosólico para formar el autofagosoma (George et al. 2000, Kametaka et al. 1996).
Esta capacidad de autólisis permite la liberación de compuestos aromáticos en el vino, especialmente nucleótidos y nucleósidos que modifican las propiedades organolépticas del producto. El flavor en vinos envejecidos sobre las lías tiene características diferentes a otros vinos, se caracterizan por poseer más cuerpo y complejidad aromática. En el caso de fermentaciones llevadas a cabo con H. vineae se ha visto que esta característica se halla resaltada respecto a las que solo tienen S. cerevisiae, probablemente porque la primera presenta lisis celular más rápida (Del Fresno et al. 2021) Otros compuestos liberados en la lisis celular son los polisacáridos que incrementan la persistencia del aroma y mejoran la sensación en boca (Loira et al. 2018) y también proteínas y ácidos grasos que influyen en la espumosidad para vinos blancos base (Gallart et al. 2002).
Conclusión
Las levaduras del género Hanseniaspora poseen cualidades muy interesantes debido a la alta producción de compuestos aromáticos distintivos. Con las nuevas herramientas de modificación genética en estas especies será más fácil describir al detalle las rutas biosintéticas para la producción de compuestos aromáticos y su regulación. Esto nos permitirá aprovechar el potencial biotecnológico de este grupo de levaduras para la producción de vinos de gran calidad con cultivos mixtos.
Agradecimientos
Agradecemos el financiamiento recibido a los proyectos CSIC Grupos números 802 y 983 de la UdelaR, Uruguay, a la Agencia Nacional de Investigación e Innovación (ANII) ANII_ALI_2_2019_1_155314, ANII_ART_2_2021_172795, ANII_2022_FCE_172630 y también a las empresas Lage y Cia (Uruguay) y Oenobrands SAS (Francia) por su apoyo para el desarrollo de nuevas levaduras del género Hanseniaspora.
Referencias
Badura, J., van Wyk, N., Brezina, S., Pretorius, I. S., Rauhut, D., Wendland, J., y von Wallbrunn, C.: “Development of genetic modification tools for Hanseniaspora uvarum”. International Journal of Molecular Sciences; 2021, 22(4), 1943. https://doi.org/10.3390/ijms22041943
Beekwilder, J., Álvarez-Huerta, M., Neef, E., Verstappen, F. W., Bouwmeester, H. J., y Aharoni, A.: “Functional characterization of enzymes forming volatile esters from strawberry and banana”. Plant Physiology; 2004, 135(4), 1865-1878. https://doi.org/10.1104/pp.104.042580
Carrau, F., Dellacassa, E., Boido, E., Medina, K., Valera, M. J., Fariña, L., Pérez, G., Martin, V., Álvarez-Valin, F. y Balestrazzi, L.: “Biology and physiology of Hanseniaspora vineae: metabolic diversity and increase flavour complexity for food fermentation”. FEMS Yeast Research; 2018, 23, foad010. https://doi.org/10.3390/fermentation4030076
Ciani, M., y Picciotti, G.: “The growth kinetics and fermentation behaviour of some non-Saccharomyces yeasts associated with wine-making”. Biotechnology Letters; 1995, 17, 1247-1250. https://doi.org/10.1007/BF00128395
D’Auria, J. C.: “Acyltransferases in plants: a good time to be BAHD”. Current opinion in plant biology; 2008, 9(3), 331-340. https://doi.org/10.1016/j.pbi.2006.03.016
Del Fresno, J. M., Escott, C., Loira, I., Carrau, F., Cuerda, R., Schneider, R., Bañuelos M.A., González C., Suárez-Lepe, J.A. y Morata, A.: “The impact of Hanseniaspora vineae fermentation and ageing on lees on the terpenic aromatic profile of white wines of the Albillo variety”. International Journal of Molecular Sciences; 2021, 22(4), 2195. https://doi.org/10.3390/ijms22042195
Del Fresno, J. M., Escott, C., Carrau, F., Herbert-Pucheta, J. E., Vaquero, C., González, C., & Morata, A.: “Improving aroma complexity with Hanseniaspora spp.: terpenes, acetate esters, and Safranal”. Fermentation, 2022, 8(11), 654. https://doi.org/10.3390/fermentation8110654
Gallart, M., López-Tamames, E., Suberbiola, G., y Buxaderas, S.: “Influence of fatty acids on wine foaming”. Journal of agricultural and Food Chemistry; 2002, 50(24), 7042-7045. https://doi.org/10.1021/jf0204452
Gallo, A., Roman, T., Paolini, M. et al.: “The co-inoculation ratio of Hanseniaspora vineae-to-Saccharomyces cerevisiae correlates with aroma metabolic features in wine”. Eur Food Res Technol., 2024, 250, 2907–2919. https://doi.org/10.1007/s00217-024-04588-8
George, M. D., Baba, M., Scott, S. V., Mizushima, N., Garrison, B. S.,Ohsumi, Y., y Klionsky, D. J.: “Apg5p functions in the sequestration step in the cytoplasm‐to‐vacuole targeting and macroautophagy pathways”. Molecular Biology of the Cell; 2000, 11, 969–982. https://doi.org/10.1091/mbc.11.3.969
Giorello, F., Valera, M. J., Martin, V., Parada, A., Salzman, V., Camesasca, L., Fariña, L., Boido, E., Medina, K., Dellacassa, E., Berna, L., Aguilar, P.S., Mas, A., Gaggero, C. y Carrau, F.: “Genomic and transcriptomic basis of Hanseniaspora vineae‘s impact on flavor diversity and wine quality”. Applied and Environmental Microbiology; 2019, 85(1), e01959-18. https://doi.org/10.3390/fermentation7030162
Guaragnella, N., Chiara, M., Capece, A., Romano, P., Pietrafesa, R., Siesto, G., Manzari, C. y Pesole, G.: “Genome sequencing and comparative analysis of three Hanseniaspora uvarum indigenous wine strains reveal remarkable biotechnological potential”. Frontiers in Microbiology; 2020, 10, 3133. https://doi.org/10.3389/fmicb.2019.03133
Heinisch, J. J., Murra, A., Jürgens, K., y Schmitz, H. P.: “A versatile toolset for genetic manipulation of the wine yeast Hanseniaspora uvarum”. International Journal of Molecular Sciences; 2023, 24(3), 1859. https://doi.org/10.3390/ijms24031859
Kametaka, S., Matsuura, A., Wada, Y., y Ohsumi, Y.: “Structural and functional analyses of APG5, a gene involved in autophagy in yeast”. Gene; 1996, 178, 139–143. https://doi.org/10.1016/0378-1119(96)00354-X
Lleixà, J., Martín, V., Portillo, M. D. C., Carrau, F., Beltran, G., y Mas, A.: “Comparison of fermentation and wines produced by inoculation of Hanseniaspora vineae and Saccharomyces cerevisiae”. Frontiers in Microbiology; 2016, 7, 338. https://doi.org/10.3389/fmicb.2016.00338
Loira, I.; Morata, A.; Palomero, F.; González, C.; Suárez-Lepe, J.A.: “Schizosaccharomyces pombe: A Promising Biotechnology for Modulating Wine Composition”. Fermentation 2018, 4, 70. https://doi.org/10.3390/fermentation4030070
Martin, V., Valera, M. J., Medina, K., Boido, E., y Carrau, F.: “Oenological impact of the Hanseniaspora/Kloeckera yeast genus on wines—A review”. Fermentation; 2018, 4(3), 76. https://doi.org/10.3390/fermentation4030076
Martin, V., Giorello, F., Fariña, L., Minteguiaga, M., Salzman, V., Boido, E., Aguilar, P.S., Gaggero, C., Dellacassa, E., Mas, A., y Carrau, F.: “De novo synthesis of benzenoid compounds by the yeast Hanseniaspora vineae increases the flavor diversity of wines”. Journal of agricultural and food chemistry; 2016, 64(22), 4574-4583. https://doi.org/10.1021/acs.jafc.5b05442
Martin, V., Valera, M. J., Medina, K., Dellacassa, E., Schneider, R., Boido, E., y Carrau, F.: “Application of Hanseniaspora vineae to improve white wine quality”. White wine technology; 2022, 99-115. https://doi.org/10.1016/B978-0-12-823497-6.00004-1
Medina, K., Boido, E., Fariña, L., Gioia, O., Gomez, M. E., Barquet, M., Gaggero, C., Dellacassa, E. y Carrau, F.: “Increased flavour diversity of Chardonnay wines by spontaneous fermentation and co-fermentation with Hanseniaspora vineae”. Food Chemistry; 2013, 141(3), 2513-2521. https://doi.org/10.1016/j.foodchem.2013.04.056
Romano, P., Fiore, C., Paraggio, M., Caruso, M., y Capece, A.: “Function of yeast species and strains in wine flavour”. International journal of food microbiology; 2003, 86(1-2): 169-180. https://doi.org/10.1016/S0168-1605(03)00290-3
Schwarz, L. V., Sandri, F. K., Scariot, F., Delamare, A. P. L., Valera, M. J., Carrau, F., & Echeverrigaray, S.: “High nitrogen concentration causes G2/M arrest in Hanseniaspora vineae”. Yeast; 2023, 40(12), 640-650. https://doi.org/10.1002/yea.3911
Schwarz, L. V., Valera, M. J., Delamare, A. P. L., Carrau, F., y Echeverrigaray, S.: “A peculiar cell cycle arrest at g2/m stage during the stationary phase of growth in the wine yeast Hanseniaspora vineae“. Current Research in Microbial Sciences; 2022, Vol.3, 100129. https://doi.org/10.1016/j.crmicr.2022.100129
Seixas, I., Santos, D., Vasconcelos, I., Mira, N. P., y Mendes-Ferreira, A.: “Insights into the transcriptional regulation of poorly characterized alcohol acetyltransferase-encoding genes (HgAATs) shed light into the production of acetate esters in the wine yeast Hanseniaspora guilliermondii”. FEMS Yeast Research; 2023, 23, foad021. https://doi.org/10.1093/femsyr/foad021
Steenwyk, J. L., Opulente, D. A., Kominek, J., Shen, X. X., Zhou, X., Labella, A. L., Bradley, N.P., Eichman, B.F., Čadež, N., Libkind, D., De Virgilio, J., Hulfachor, A.B., Kurtzman, C.P., Hittinger, C.T. y Rokas, A.: “Extensive loss of cell-cycle and DNA repair genes in an ancient lineage of bipolar budding yeasts”. PLoS Biology; 2019, 17(5), e3000255. https://doi.org/10.1371/journal.pbio.3000255
Valera, M. J., Olivera, V., Boido, E., Dellacassa, E., y Carrau, F.: “Wine aroma characterization of the two main fermentation yeast species of the apiculate genus Hanseniaspora”. Fermentation; 2021, 7(3),162. https://doi.org/10.3390/fermentation7030162
Van Laere, S. D., Saerens, S. M., Verstrepen, K. J., Van Dijck, P., Thevelein, J. M., y Delvaux, F. R.: “Flavour formation in fungi: characterisation of KlAtf, the Kluyveromyces lactis orthologue of the Saccharomyces cerevisiae alcohol acetyltransferases Atf1 and Atf2.” Applied microbiology and biotechnology; 2008, 78, 783-792. https://doi.org/10.1007/s00253-008-1366-9
Van Wyk, N., Badura, J., von Wallbrunn, C., y Pretorius, I. S.: “Exploring future applications of the apiculate yeast Hanseniaspora”. Critical Reviews in Biotechnology; 2023, 44(1), 100-119. https://doi.org/10.1080/0 7388551.2022.2136565
Versini, G., Carlin, S., Nicolini, G., Dellacassa, E., & Carrau, F.: “Updating of varietal aroma components in wines. In Vitiviniculture in the Southern emisphere: proceedings of the 7th Latin-American Congress of viticulture and winemaking, Mendoza, Argentina, 28 November-3 December” 1999 (pp.323-349). http://hdl.handle.net/10449/16492
Zhang, P., Zhang, R., Sirisena, S., Gan, R., y Fang, Z.: “Beta-glucosidase activity of wine yeasts and its impacts on wine volatiles and phenolics: A mini-review”. Food Microbiology; 2021, 100, 103859. https://doi.org/10.1016/j.fm.2021.103859