Los pigmentos responsables del color de los vinos tintos proceden de la materia prima con que se elaboran, las uvas, y se localizan de forma exclusiva en los hollejos y ocasionalmente también en la pulpa de las variedades denominadas tintoreras. Estos pigmentos rojos son unos compuestos fenólicos que se denominan antocianos y, en la uva, se encuentran únicamente como antocianos monómeros, no ligados a otras moléculas. Realmente hay que hablar de «pigmentos del vino», en plural, pues los antocianos monómeros originales de la uva tienen una vida efímera en el vino, de sólo unos meses, y desaparecen para dar lugar a nuevos pigmentos, de muy variadas estructuras y que llegan a tener una persistencia de muchos años, como resultado de las reacciones químicas espontáneas de los antocianos monómeros con otros componentes del vino, algunos procedentes también de la uva y otros de las levaduras o generados durante la crianza en barricas.
Fenómenos implicados en la transferencia de color durante la vinificación
Se puede considerar que la transferencia de antocianos monómeros de la uva al vino es un equilibrio de reparto de estas sustancias entre dos fases inmiscibles, una sólida (el hollejo de las uvas) y otra líquida (el mosto o vino en fermentación). Como en todo proceso de reparto entre fases, el equilibrio alcanzado dependerá de la afinidad de las sustancias a repartir por las dos fases entre las que se transfieren. La solubilidad de los antocianos monómeros en el medio acuoso que es el mosto (vino en fermentación), es la fuerza motriz que inicialmente determina su transferencia durante la vinificación. La transferencia de los compuestos fenólico, en general, también está sometida a este tipo de equilibrios de reparto.
| Tabla 1 Factores ensayados para la mejora del color en vinos tintos | |
| Prefermentativos | Fermentativos |
| – Disminución del pH del mosto – Aumento de la cantidad de SO2 añadido – Variación de la temperatura previa a la fermentación: termovinificación; criomaceración; flash-expansión – Adición de enzimas pectolíticos |
– Duración y tipo de maceración: bazuqueos; remontados; deléstage; fermentadores rotatorios; fermentadores Ganimede; etc. – Uso de agentes clarificantes – Adición de manoproteínas |
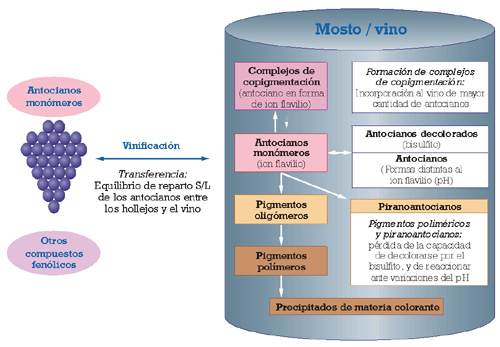
Son numerosos y muy diversos los factores que se han estudiado y que aún se ensayan, para intentar mejorar los porcentajes de transferencia de los antocianos monómeros durante la vinificación (Tabla 1). Resulta llamativo constatar que, ante tal diversidad de factores ensayados, hasta la fecha no se haya podido establecer un método universal para la mejora de la extracción del color durante la elaboración de vino tinto. Además, muchos de los factores ensayados no son selectivos en cuanto a la transferencia de antocianos monómeros, y aunque consiguen un aumento efectivo del color del vino, pueden provocar efectos secundarios indeseables, como un aumento de la astringencia por una transferencia excesiva de cierto tipo de taninos de las pepitas de las uvas. Tal vez esta situación sea un reflejo de la falta de conocimiento que aún se tiene de lo que ocurre, a nivel molecular, en los procesos implicados en la transferencia de color del vino y en otros procesos que interfieren con éstos y que implican no sólo a los pigmentos sino también a otros compuestos fenólicos disueltos en el mosto, y sobre cuyo esclarecimiento se trabaja activamente en los últimos años.1 En la figura 1 se han esquematizado los procesos implicados en la extracción de color durante la vinificación y en la posterior evolución del color durante el envejecimiento del vino tinto.
La copigmentación y su relación con el aumento y estabilización del color de los vinos tintos
Origen y efectos de la copigmentación en los vinos
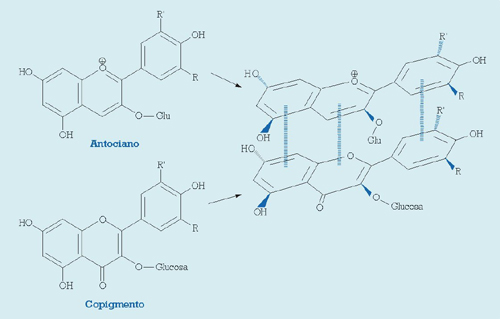
La copigmentación es un fenómeno que se produce típicamente en medio acuoso y que afecta a los antocianos monómeros en su forma de catión flavilio (los pigmentos), a la vez que a otros compuestos fenólicos, normalmente no pigmentados, denominados copigmentos o cofactores de copigmentación.2 Desde un punto de vista molecular, el fenómeno consiste en la formación de un complejo de estequiometría 1:1, en el que un pigmento (con estructura plana) se apila con un copigmento (también necesita tener una estructura plana para ello), como si de un sándwich se tratara, estableciéndose unas débiles interacciones entre las nubes electrónicas de los anillos aromáticos de ambos (fig. 2). La copigmentación puede, a su vez, subdividirse en tres categorías, según la naturaleza del copigmento implicado:
- Copigmentación intermolecular: el copigmento es una molécula de naturaleza distinta al antociano monómero, como una molécula de flavonol, por ejemplo.
- Copigmentación intramolecular: el copigmento es una porción de la propia molécula de antociano monómero, como puede ser el caso del sustituyente cumaroilo de un antociano cumarílico.
- Autoasociación: en este caso el copigmento es otra molécula de antociano monómero.
Los complejos de copigmentación se forman con mucha facilidad (se han medido constantes de complejación del orden de 102 – 103 mol L-1), pero también se disocian fácilmente, por ejemplo diluyendo suficientemente o aumentando la proporción de ciertos cosolventes en el medio acuoso, como el propio etanol del vino o el ácido acético que también puede encontrarse en éste.3 Los mejores copigmentos son los compuestos fenólicos denominados flavonoles, pero en las uvas y en los vinos éstos se encuentran en pequeñas cantidades. Otros copigmentos de naturaleza fenólica encontrados en los vinos son los ácidos hidroxicinámicos (ácidos cafeico, p-cumárico y ferúlico), también en pequeñas cantidades. En cambio, los compuestos fenólicos más abundantes de los vinos tintos, los flavan-3-oles (monómeros como la (+)-catequina y la (-)-epicatequina, oligómeros como las proantocianidinas tipo B y polímeros como los taninos), son copigmentos poco efectivos.
La formación del complejo de copigmentación provoca dos efectos que habitualmente se observan asociados al fenómeno de la copigmentación:
- Un efecto hipercrómico, es decir, un incremento de la intensidad del color rojo mostrado por el vino tinto con copigmentación.
- Un efecto batocrómico, es decir, un viraje hacia tonalidades más azuladas del color rojo del vino tinto.
Ambos efectos se suelen manifestar simultáneamente en los vinos tintos, sobre todo en los jóvenes, en diverso grado, según la composición fenólica y las relaciones molares de copigmento/pigmento que de forma particular se producen en un vino.4
Cómo incrementar la copigmentación en los vinos tintos
Para fomentar la copigmentación en los vinos jóvenes, y que sus efectos sean más notables y duraderos, es necesario que en los vinos haya una mayor concentración de copigmentos, sobre todo de los más importantes, los flavonoles, así como que la relación molar copigmento/pigmento pueda ser aumentada. Para lograr estos objetivos, son posibles varias estrategias, que se pueden enfocar desde una doble perspectiva.
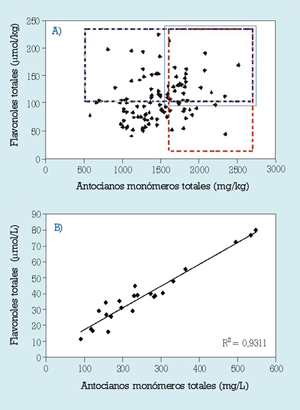
En el ámbito de la viticultura, habría que tratar de conseguir unas uvas tintas que tuvieran simultáneamente el mayor contenido posible en pigmentos (antocianos monómeros) y en los mejores copigmentos (flavonoles). Puesto que la síntesis de los antocianos y la de los flavonoles en la uva ocurre de forma independiente, tanto espacial como temporalmente, las distintas partidas de uvas que llegan a una bodega pueden ser muy heterogéneas en su composición en antocianos y en flavonoles (fig. 3A). Si en la bodega seleccionamos las uvas sólo por su alto contenido en antocianos (línea discontinua roja), hallaremos partidas a las que no les podamos extraer todo su potencial de color, por tener un bajo contenido en flavonoles. De forma contraria, podríamos escoger únicamente aquellas uvas que tuvieran un alto contenido en flavonoles (línea discontinua azul), pero encontraríamos entonces una gran variabilidad en el contenido en antocianos. Las partidas de uvas más interesantes serían las que cumpliesen simultáneamente ambos requisitos (línea continua). Para ello se hace indispensable el análisis de las uvas en relación no sólo a su contenido en antocianos (absorbancia a 520 nm), como ya se está haciendo en muchas bodegas, sino también en compuestos flavonoideos, especialmente en flavonoles (absorbancia a 360 nm).
En el ámbito de la enología, la estrategia para incrementar la copigmentación consistiría en aumentar las relaciones molares de copigmento/pigmento, para lo cual ya se han ensayado algunas posibilidades, que podrían agruparse en:
- Adición prefermentativa de copigmentos. La adición de sustancias puras permite obtener vinos tintos de mayor intensidad de color rojo, estando sus antocianos monómeros más protegidos frente a la desaparición durante el envejecimiento.5 También se podría probar con extractos procedentes de la propia uva (hollejos) o de otras fuentes naturales. Esta posibilidad plantea problemas legales debido a la prohibición de usar otros ingredientes distintos a las uvas o a sus mostos en la elaboración de vino.
- Cofermentación de uvas distintas. Se trataría de compensar la falta de copigmentos en uvas con alto contenido en antocianos con otras uvas que fueran excedentarias para los primeros. En principio, cabe imaginar la cofermentación de uvas tintas de igual o de diferente variedad, pero también la cofermentación de uvas tintas con uvas blancas (como se viene haciendo tradicionalmente en algunas zonas de Italia, Francia, España o Argentina) o, mejor aún, con los hollejos de uvas blancas para no diluir las concentraciones de antocianos y flavonoles. Un argumento acerca de las mejoras que podría introducir la cofermentación de uvas de la misma variedad se muestra en la figura 3B. En ésta se puede ver cómo, a partir de unas uvas tan heterogéneas como las de la figura 3A, los vinos tintos jóvenes elaborados a partir de ellas guardaron, en contraste, una muy buena correlación entre sus contenidos en antocianos y en flavonoles, gracias al fenómeno de la copigmentación. Es decir, la copigmentación parece ejercer un papel de fuerza motriz adicional en la transferencia de antocianos monómeros durante la fermentación.
Estabilización del color por formación de pigmentos poliméricos durante el envejecimiento
Los antocianos monómeros son unos pigmentos inestables cuyo color cambia en función del pH del medio, y además son decolorables por el bisulfito. Durante su envejecimiento, los vinos tintos van perdiendo intensidad en su color rojo, y la tonalidad de éste va cambiando del rojo-púrpura hacia el rojo-anaranjado. Mientras los vinos tintos jóvenes se decoloran en gran medida por el bisulfito, los vinos tintos envejecidos apenas pierden color con este reactivo; a la par, el color rojo de los vinos envejecidos cada vez se afecta menos por cambios en el pH; por ambas razones se dice que el color del vino tinto se estabiliza durante su envejecimiento. Paralelamente, se observa que la magnitud del fenómeno de copigmentación va disminuyendo y, prácticamente, sus efectos sobre el color total del vino resultan inapreciables después de unos meses de envejecimiento.4,5
La evolución y estabilización del color de los vinos tintos durante su envejecimiento han sido atribuidas clásicamente a la formación de pigmentos poliméricos, por reacción entre los antocianos monómeros y los compuestos fenólicos mayoritarios de los vinos tintos, los flavan-3-oles (taninos). En principio, son posibles dos tipos de pigmentos poliméricos (fig. 4), uno en los que la molécula de antociano ocupa la posición inicial del polímero (pigmento tipo A-T), y otro en los que el antociano es la parte final de éste (pigmento tipo T-A). Se sabe que el acetaldehído (un metabolito secundario de las levaduras, y un producto que también se forma lentamente en la crianza en barrica de roble por oxidación química del etanol) acelera la formación de estos pigmentos antociánicos poliméricos, actuando de nexo de unión entre los antocianos y los taninos.
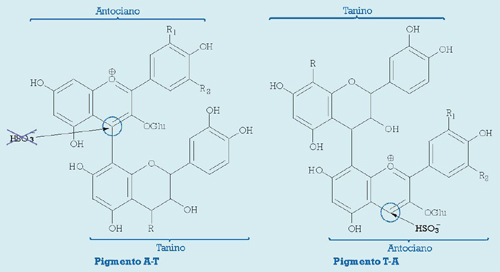
La formación de pigmentos poliméricos permite explicar la pérdida de intensidad colorante del vino tinto durante el envejecimiento, pues a mayor grado de polimerización, estos pigmentos se vuelven insolubles y terminan por precipitar formando los depósitos de materia colorante observados en los vinos envejecidos. También se puede explicar el viraje en la tonalidad del color de los vinos tintos durante el envejecimiento, pues los cromóforos iniciales (los antocianos monómeros) desaparecen y ya no pueden formar complejos de copigmentación, perdiéndose las tonalidades púrpuras del color rojo de los vinos, asociadas al efecto batocrómico de la copigmentación. La desaparición de la copigmentación también explica la disminución en intensidad colorante, sin necesidad de formación de depósitos de materia colorante, al perderse el efecto hipercrómico asociado a la copigmentación. Por último, la formación de este tipo de pigmentos poliméricos también explica la estabilización del color: tanto la decoloración por bisulfito como los cambios de color asociados a la variación del pH (que a partir de la forma flavilio comienzan con la hidratación), necesitan tener libre la posición C-4 del anillo de pirano del antociano, que es por donde éste reacciona con el anión bisulfito o el anión hidroxilo del agua; en los pigmentos del tipo A-T esta posición está ya bloqueada por la unión entre la molécula de antociano y la de tanino, por lo que este tipo de pigmento es estable; en cambio, los pigmentos del tipo T-A aún mantienen libre esta posición y se pueden decolorar.
Piranoantocianos: una vía adicional de estabilización del color en vinos envejecidos
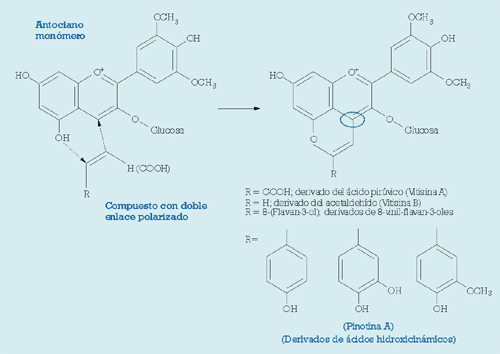
Primero en sistemas modelo, y posteriormente en los vinos tintos envejecidos, en los últimos años se han aislado e identificado una serie de pigmentos derivados de los antocianos monómeros que se caracterizan por poseer un anillo de pirano adicional que está fusionado con el esqueleto flavonoideo del catión flavilio del antociano original. Por esta razón, estos nuevos pigmentos han sido denominados piranoantocianos y, hoy parece claro que la formación de este tipo de pigmentos antociánicos constituye una vía adicional, y bastante general, a la clásica formación de pigmentos poliméricos entre antocianos y taninos, en el proceso de estabilización del color durante el envejecimiento de los vinos tintos. Para la formación de un piranoantociano, es necesario que un antociano monómero reaccione con una sustancia que contenga un doble enlace polarizado (fig. 5), es decir, con sustituyentes de diferente polaridad en ambos extremos del doble enlace.
La primera estructura de piranoantociano que se identificó procedía de la reacción del 3-monoglucósido de malvidina con el ácido pirúvico (un metabolito secundario de las levaduras), a través de la forma enólica de este último (el enol es el doble enlace polarizado), y posterior descarboxilación, y fue denominado Vitisina A.6 Posteriormente, ha sido identificado un piranoantociano denominado Pinotina A,7 encontrado en vinos de la variedad pinot noir y formado a partir del ácido cafeico, un ácido hidroxicinámico.
Los piranoantocianos son unos pigmentos antociánicos no decolorables por el bisulfito y bastante estables ante variaciones de pH, porque también tienen bloqueada la posición C-4 del anillo de pirano flavonoideo. Al contrario que los pigmentos poliméricos, que normalmente se encuentran en un estado coloidal en el vino y tienen tendencia a precipitar, los piranoantocianos son moléculas de un tamaño fijo y similar a la de los antocianos monómeros de los que derivan y se mantienen disueltos en el vino, por lo que tendrán poca tendencia a perderse en los precipitados de materia colorante que se forman en los vinos tintos envejecidos, o a quedarse retenidos en los filtros por los que se pasan los vinos antes de su embotellado.
Otra característica interesante de los piranoantocianos es que poseen un cromóforo distinto al de los antocianos monómeros, con distintas propiedades. Mientras los antocianos monómeros son unos pigmentos de color rojo (máximo de absorción a 520 nm para el 3-monoglucósido de malvidina, en medio acuoso a pH 1,5), los piranoantocianos lo son de color rojo-anaranjado (máximos de absorción sobre 498 – 512 nm en medio acuoso a pH < 2), la misma tonalidad de color que suelen mostrar los vinos tintos envejecidos. Además, mientras los antocianos monómeros son unos pigmentos que poseen unos cromóforos potentes (el coeficiente de absorción molar a 520 nm para el 3-monoglucósido de malvidina, a pH 1,5 es de 27000 L g-1 cm-1) y que incrementan su intensidad colorante al formar complejos de copigmentación, los piranoantocianos poseen unos cromóforos más débiles, con unos valores de coeficientes de absorción molar a 520 nm, a pH 1,5, del orden de la mitad –o menos– de los correspondientes a los antocianos monómeros de los que derivan.8 Por tanto, para concentraciones molares iguales, los piranoantocianos otorgan menor intensidad colorante y una tonalidad roja más anaranjada que los correspondientes antocianos monómeros.
Por último, inicialmente se propuso que la formación de piranoantocianos derivados de los ácidos hidroxicinámicos ocurría a través de los 4-vinilfenoles formados por descarboxilación, catalizada enzimáticamente por los microorganismos implicados en la fermentación alcohólica. No obstante, si bien se han encontrado levaduras con esta actividad enzimática, no son activas frente al ácido cafeico, y hace poco se demostró la formación de piranoantocianos por reacción directa entre los ácidos hidroxicinámicos y los antocianos monómeros.9 Muy recientemente se ha comprobado que, en vinos tintos de la variedad garnacha, la formación de piranoantocianos derivados de los ácidos hidroxicinámicos ocurre en dos etapas:10 durante la fermentación alcohólica se forman pequeñas cantidades de los piranoantocianos derivados de los ácidos p-cumárico y ferúlico, por vía enzimática, que implicaría la hidrólisis de los precursores (ácidos cutárico y fertárico, respectivamente) y la posterior descarboxilación que originaría los muy reactivos 4-vinilfenoles; en una segunda fase, tras la fermentación maloláctica y algunos meses de envejecimiento, se observa la hidrólisis de los precursores de los ácidos cafeico, p-cumárico y ferúlico (ácidos caftárico, cutárico y fertárico, respectivamente) y la reacción directa de éstos con los antocianos.
Los resultados anteriormente expuestos sugieren nuevas vías para lograr vinos con una mayor proporción de pigmentos estables del tipo piranoantocianos, como podrían ser el empleo de variedades de uva ricas en precursores de los ácidos hidroxicinámicos, junto con el fomento de la hidrólisis de sus precursores durante las primeras fases de envejecimiento de los vinos tintos.
Bibliografía
1 «Red Wine Color. Revealing the Mysteries», A.L. Waterhouse y J.A. Kennedy, Eds., ACS Symposium Series 886. American Chemical Society: Washington, DC, 2004.
2 Boulton, R.: «The copigmentation of anthocyanins and its role in the color of red wine: a critical review», Am J Enol Viticult 2001; 52: 67-87.
3 Hermosín Gutiérrez, I.: «Influence of ethanol content on the extent of copigmentation in a Cencibel young red wine», J Agric Food Chem 2003; 51: 4079-4083.
4 Hermosín Gutiérrez, I.; Sánchez-Palomo Lorenzo, E. y Vicario Espinosa, A.: «Phenolic composition and magnitude of copigmentation in young and shortly aged red wines made from the cultivars Cabernet Sauvignon, Cencibel, and Syrah», Food Chem 2005; 92: 269-283.
5 Schwarz, M.; Picazo-Bacete, J.J.; Winterhalter, P. y Hermosín-Gutiérrez, I.: «Effect of copigments and grape cultivar on the color of red wines fermented after the addition of copigments», J Agric Food Chem 2005; 53: 8372-8381.
6 Fulcrand, H.; Cameira dos Santos, P.J.; Sarni-Manchado, P.; Cheynier, V. y Favre-Bonvin, J.: «Structure of new anthocyanin-derived wine pigments», J Chem Soc Perkin Trans 1 1996: 735-739.
7 Alberto, M.R.; Farías, M.E. y Manca de Nadra, M.C.: «Effect of gallic acid and catechin on Lactobacillus hilgardii 5w growth and metabolism of organic compounds», J Agric Food Chem 2001; 49: 4359-4363.
8 Håkansson, A. E.; Pardon, K.; Hayasaka, Y.; de Sa, M. y Herderich, M.: «Structures and colour properties of new red wine pigments», Tetrahedron Lett 2003; 44: 4887-4891.
9 Schwarz, M.; Wabnitz, T. C. y Winterhalter, P.: «Pathway leading to the formation of anthocyanin-vinylphenol adducts and related pigments in red wines», J Agric Food Chem 2003; 51: 3682-3687.
10 Rentzsch, M.; Schwarz, M.; Winterhalter, P. y Hermosín-Gutiérrez, I.: «Formation of hydroxyphenyl-pyranoanthocyanins in Grenache wines: precursor levels and evolution during aging», J Agric Food Chem (en prensa).