La elaboración de vino en depósitos de madera, su almacenaje y transporte en barricas se conoce desde tiempos del Imperio romano. Se podría suponer, por tanto, que la gran experiencia acumulada por la observación durante 2000 años de la evolución del vino en estos recipientes hubiera desentrañado y explicado los cambios que se producen y las razones de los mismos.
Sin embargo, a pesar de los precedentes la deducción que se desprende de la reflexión anterior no es correcta, ya que, a pesar de las muchas experiencias adquiridas y estudios realizados, la crianza del vino en barrica sigue siendo un tema de gran actualidad. Esto es así no sólo por su impacto económico, sino por razones científicas entre las que podemos destacar la predicción del comportamiento de los diferentes vinos en las barricas, la predicción y definición de su perfil sensorial y la demostración analítica de sus diferencias sensoriales y de composición en relación con otros vinos que han estado en contacto con madera pero no en barricas.
El impacto económico es claro por el coste de las barricas, su mantenimiento y buena utilización, aspectos de los que todo el mundo parece ser consciente. No obstante no ocurre lo mismo con el envejecimiento del vino. Este es un proceso de muy difícil interpretación por su complejidad, sobre todo en vinos de gran calidad y, a pesar de que en la bibliografía figuran numerosos trabajos, todavía no se han elaborado hipótesis que expliquen la totalidad del proceso evolutivo o, al menos, no se han aceptado plenamente.
A pesar de estas limitaciones, se sabe que en la crianza del vino ocurren los fenómenos siguientes:
- Entrada de aire a través de la madera o de los trasiegos.
- Pérdida de vino y evaporación de componentes volátiles a través de la madera o de los trasiegos.
- Precipitación de diversas sustancias del vino en la barrica.
- Cesión de sustancias contenidas en la madera.
- Formación y degradación de compuestos en los vinos.
- Transformación de polifenoles en los vinos.
- Adsorción de odorantes por la madera.
En relación con los cambios que experimenta el aroma del vino en su crianza, hay muchas preguntas todavía sin respuesta:
► La razón de la diferente capacidad de diversos vinos monovarietales de extraer compuestos volátiles de la madera. Este hecho indica que el paso de sustancias de la madera al vino es más complejo de lo que es una extracción simple. Esto es un hecho bien demostrado.
► La proporción de compuestos como vainillina, eugenol, furfural, cis-whiskylactona, guayacol y 4-alil-2,6-dimetoxifenol que provienen de la madera de la barrica y los que provienen de precursores aromáticos de la uva.
► La capacidad de la madera de ceder b-ionona.
► El papel sensorial efectivo de algunos de los compuestos o familias de compuestos que cede la madera.
► Las diferencias de comportamiento de las barricas de roble según su especie-origen, el secado de la madera, su tostado y volumen.
► El papel sensorial de compuestos generados por oxidación o hidrólisis de precursores, así como la modificación sensorial por la disminución o desaparición de sustancias por evaporación o adsorción.
A estas preguntas se podría añadir otra que es clave para muchos enólogos: ¿cuál es el tiempo de vida de una barrica desde el punto de vista de la crianza?
Durante los últimos años se ha estudiado de una forma sistemática en el Laboratorio de Análisis del Aroma y Enología el comportamiento del vino en la barrica intentando contestar a algunas de las cuestiones planteadas. Esos trabajos han constituido la Tesis Doctoral de la Dra. Margarita Aznar.1 y de la Dra. Idoya Jarauta.2 Alguno de sus resultados se incluyen en esta exposición que comenzamos con la enumeración de los compuestos que cede la barrica, su origen e importancia sensorial.
Compuestos cedidos por la madera
La madera no es un material inerte, sino un producto natural que contiene, entre otras sustancias, aromas y compuestos fenólicos no volátiles que son responsables de modificaciones que sufre el vino durante su estancia en la barrica. Por esta razón muchos investigadores han trabajado en identificar estos compuestos extrayéndolos, tanto con disolventes orgánicos, como con disoluciones hidroalcohólicas y vino.3-6 Boidron et al.6 en 1988 clasificaron las sustancias volátiles extraídas en las familias siguientes: derivados furánicos, lactonas, fenoles volátiles, fenilcetonas y aldehídos fenólicos. A ellas nos vamos a referir.
Derivados furánicos
Se engloban en este grupo: furfural, 5-metilfurfural, 5-hidroximetilfurfural y furfuril alcohol. Estas sustancias se generan en su mayor parte durante la etapa del tostado de la barrica como consecuencia de una reacción de Maillard de los compuestos glucídicos de la madera. El furfural proviene de las pentosas7 y el 5-metilfurfural y el 5-hidroximetilfurfural de las hexosas. El furfuril alcohol se forma por reducción enzimática de sus análogos aldehídos durante el envejecimiento. En consecuencia, los factores relativos a la actividad enzimática, como pH y temperatura, afectarán a su concentración.7-9
Lactonas
Las más importantes son la cis y trans-whiskylactonas. Estos compuestos se encuentran ya en la madera verde y su concentración en la barrica depende del tostado y del origen del roble.6-9 También se han encontrado en vinos blancos sin crianza, por lo que su aparición en el vino podría tener otro origen.10
Fenoles volátiles
La madera no tostada contiene fenoles volátiles en proporciones pequeñas, siendo el eugenol el compuesto más característico.6,10 Como consecuencia del tostado, de la degradación térmica de la lignina, se generan guayacol, fenol, para-cresol, orto-cresol, 4-metilguayacol, 4-propilguayacol y 4-alil-2,6-dimetoxifenol.6-8, 12 Además, tanto el fenol como el o- y p-cresol pueden tener un origen microbiológico.13
Asimismo tienen origen microbiológico otros fenoles volátiles importantes, como el 4-etilfenol y el 4-etilguayacol.14 Levaduras del género Brettanomyces y Dekkera, en presencia de ácidos para-cumárico y ferúlico, sintetizan el 4-etilfenol y 4-etilguayacol, respectivamente. Esto lo realizan por medio de las enzimas cinamato descarboxilasa, que transforma los ácidos cinámicos en los correspondientes vinilfenoles y la vinilreductasa que cataliza la reducción de los vinilfenoles a etilfenoles.
Fenilcetonas
A esta familia pertenecen acetovainillona, propiovanillona y butirovanillona. La madera verde contiene pocas fenilcetonas pero el tostado aumenta su concentración.6
Aldehídos fenólicos
Se engloban en este grupo vainillina, siringaldehído, coniferaldehído y sinapaldehído. Estos aldehídos se generan por la degradación térmica de la lignina durante el tostado, por extracción de los monómeros libres presentes en la lignina y a través de la etanólisis de la lignina.13
El tostado aumenta considerablemente la cantidad de vainillina y, sobre todo, de siringaldehído.
Papel sensorial efectivo de alguno de los compuestos o familia de compuestos que cede la madera
Cuando se revisa la bibliografía sobre la crianza del vino y se busca el impacto sensorial de las sustancias que aportan las diferencias con el vino que no ha tenido contacto con la madera, llama poderosamente la atención la ausencia de información verdaderamente útil. Hay muchos estudios sobre la cesión de tales compuestos, puesta de manifiesto por medio del análisis químico, pero hay grandes discrepancias sobre sus efectos. Para atribuir la importancia sensorial se han usado los umbrales de detección y los valores de aroma. Y aquí surge la dificultad de interpretar los resultados, ya que en la bibliografía figuran datos muy dispares de los umbrales de percepción. Además, los valores reseñados se refieren casi siempre a productos puros, sin tener en cuenta los efectos sinérgicos y antagónicos entre compuestos.
Por otra parte, y con más frecuencia de la deseada, aparecen descriptores en el vino que corresponden al aroma de compuestos puros, pero el valor de aroma de tales compuestos en ese vino es muy inferior a la unidad, por lo que no puede explicarse su olor, únicamente por un efecto sinérgico. Es muy posible que la mezcla de olores diferentes, en ciertas proporciones, conduzca a un aroma que recuerde, o coincida, con el de un compuesto que cede la barrica y se asigne a tal sustancia una importancia sensorial que no tiene.
En la tabla 1 se indican los descriptores y umbrales de detección de compuestos que cede la barrica. Se han agrupado según las familias de compuestos anteriormente citadas.
Tabla 1 Valores umbral* de diferentes compuestos extraídos de la bibliografía
Aldehído-cetona |
Descriptor |
Umbral (mgL-1) |
Ref. bibliogr. |
||
| Furfural | Almendra4 | 8a:15b:65c:20d
14,1a |
4, 13, 40, 41
38 |
||
| 5-metilfurfural | Almendra tostada4 | 6a:16b:52c:45d | 4, 13, 40, 41 | ||
| 5-hidroximetilfurfural | Almendra | 0,09b | 40 | ||
| Furfuril alcohol | Heno, moho4 | 1a:15b:35c:45d | 4, 13, 40 | ||
| b-damascenona | Manzana asada24 | 0,05×10-3 d
0,05×10-3 d |
25, 43
44 |
||
| b-ionona | Violetas12,47 | 0,0045×10-3 d
0,09×10-3 b |
25
25 |
||
Lactonas |
Descriptor |
Umbral (mgL-1) |
Ref. bibliogr. |
||
| cis-whiskylactona | Coco, madera13 | 0,028a:0,025b:0,092c:0,074d
0,035 b 0,067 b |
13
45 25, 43 |
||
| trans-whiskylactona | Coco, madera13 | 0,064a:0,11b:0,46c:0,32d
0,122 b 0,79 |
13
45
|
||
| cis + trans– whiskylactona | Coco, madera4 | 0,02a:0,015b:0,12c:0,125d | 4 | ||
| g-octalactona | Melocotón | 0,035 | 40 | ||
| g-nonalactona | Coco, graso13 | 0,07b
0,03d |
40
25, 43, 46 |
||
| d-nonalactona | Graso | 2,6 d | 25 | ||
| g-decalactona | Melocotón | 0,088 a
1 b |
25, 43
41 |
||
| d-decalactona | Melocotón | 4,2 d
0,386 b |
25
43 |
||
Aldehídos fenólicos y derivados |
Descriptor | Umbral (mgL-1) |
Ref. bibliogr. |
||
| Vainillina | Vainilla4 | 0,105a:0,065b:0,4c:0,32d
2a:0.5b 0,015 b 0,1-4 a 0,2 b 0,995 b |
4, 13
20 45 25 44 |
||
| Siringaldehído | > 50a | 4, 13 | |||
| Acetovainillona | Vainilla13 | 3a:15b:25c:25d
5b 1b |
13
47 |
||
| Vainillato de etilo | Vainilla13 | 1,3a:2,5b:8,5c:8d
0.99b |
13
47 |
||
| Vainillato de metilo | Vainilla | 3b | 48 | ||
Fenoles volátiles |
Descriptor |
Umbral (mgL-1) |
Ref. bibliogr. |
||
| Guayacol (2-metoxifenol) | Humo4 | 0,0055a:0,02b:0,095c:0,075d
0,013a:0,003 b 0,01a |
4,13
25 35 |
||
| 4-metilguayacol (4-metil-2-metoxifenol) | Quemado4 | 0,01a:0,03b:0,065c:0,065d | 4, 13 | ||
| 4-etilguayacol (4-etil-2-metoxifenol) | Especiado4 | 0,025a:0,047b:0,07c:0,15d
0,14d 0,033b |
4, 13, 12
24 25, 43 |
||
| 4-vinilguayacol (4-vinil-2-metoxifenol) | Pimienta, clavo4 | 0,032a:0,13b:0,44c:0,38d
1.1b |
4, 13
43 |
||
| 4-vinilfenol | Medicinal | 0,085a:0,18b:0,77c:1.5d | 4, 43 | ||
| Isoeugenol II | Especia | 0,006b | 47 | ||
| Eugenol (4-alil-2-metoxifenol) | Clavo4 | 0,007a:0,015b:0,1c:0,5d
0,015b 0,011b 0,005b 0,0095b 0,006b |
4, 13
45 25 44, 41 48 43 |
||
| o-cresol (2-metilfenol) | Betún4 | 0,045a:0,12b:0,06c:0,8d
0,031b |
4, 13
25 |
||
| p-cresol | Medicinal25 | 0,01b | 25 | ||
| m-cresol (4-metilfenol) | Farmacéutico4 | 0,085a:0,2b:0,38c:0,18d
0,068b |
4, 13
25 |
||
| Fenol | Tinta4 | 5,5a:15b:35c:25d | |||
| 4-etilfenol | Caballo4 | 0,13a:0,44b:1.1c:1.2d
1a:0,14b 0,62d
|
4, 13, 12
25, 41 12 |
||
| Siringol (2,6-dimetoxifenol) | Humo13 | 0,4a:1,7b:1,5c:2d | 4, 13 | ||
| 4-alil-2,6-dimetoxifenol | Especiado, humo13 | 1,2a:3b:12c:9d
|
4, 13, 42 | ||
| 4-propilguayacol | Fenólico47 | 0,01b | 23 | ||
| 2,6-dimetoxifenol</span | Medicinal47 | 1,7b
0,57b
|
13
48 |
||
Enolonas |
Descriptor | Umbral (mgL-1) |
Ref. bibliogr. |
||
| Furaneol (4-hidroxi-2,5-dimetil-4H-piran-4-ona) | Caramelo50 | 0,2b
0,12b 0,5b 0,7b |
1
40 44 |
||
| Cicloteno (2-hidroxi-3-metil-2-ciclopenten-1-ona) | Caramelo50 | 2b | 1, 40 | ||
| Maltol (3-hidroxi-2-metil-4H-piranona) | Caramelo50 | 5b | 1, 40 | ||
| Dihidromaltol (2,3-dihidro-5-hidroxi-6-metil-4H-piran-4-ona) | Caramelo50 | ||||
| Sotolón | Dulce, nuez25 | 0,01b
0,0025a 0,005b 0,009b |
40, 45
25, 49 44, 41 |
||
| Homofuraneol | Caramelo46 | 0,055b
0,5b 0,125b |
40
44 |
||
* El umbral se refiere a diferentes matrices: a) agua, b) solución modelo, c) vino blanco, d) vino tinto
Como puede verse el número de compuestos indicados en la tabla es mayor que el de citados con anterioridad. Esto se debe a que hasta hace poco tiempo no se conocía la importancia sensorial de los mismos en el vino y, por tanto, no se le daba importancia. En la actualidad, se sabe que son importantes para el aroma del vino y por esa razón los incluimos.
Los derivados furánicos se hallan normalmente por debajo de su umbral de olfacción,6,15,19 por lo que no deberían ser importantes desde el punto de vista sensorial. Sin embargo, se ha señalado16 que el furfural tiene un efecto modificante importante en la percepción de las whiskylactonas.
Las whiskylactonas se hallan en los vinos de crianza en concentraciones superiores a su umbral de percepción y son contribuyentes importantes al aroma de estos vinos, sobre todo el isómero cis. En barricas nuevas llega a tener 15 unidades de valores de aroma. Las whiskylactonas se relacionan con el aroma a coco del vino chardonnay, con el aroma a coco, vainilla, cereza, chocolate negro del cabernet sauvignon y, en general, con el aroma a madera descrito en un sentido positivo, ya que los paneles de cata dan valoraciones más altas a los vinos con mayores concentraciones de estas lactosas. No obstante, la calidad sensorial disminuye cuando tal concentración es excesiva; por encima de 235 mg L-1 de cis-whiskylactona la percepción del olor cambia a aromas resinosos y de barniz.20
Los fenoles volátiles desempeñan un papel importante en el aroma del vino. A las cantidades ya presentes en los vinos tintos se suman las aportadas por la barrica y se superan los umbrales de percepción. El guayacol es el responsable de la nota a ahumado y el eugenol a la de especias y más concretamente a clavo.
Los compuestos 4-etilfenol y 4-etilguayacol son responsables de olores no deseados para la buena calidad del vino, como son los aromas fenólicos, animal y establo. Por otra parte poseen una acción inhibidora de la percepción de olores positivos, como los de las familias anteriormente descritas, por lo que su presencia, a partir de cierta concentración no es positiva en ningún caso.
Las fenilcetonas, en especial la acetovainillona, supera en los vinos el umbral de detección, por lo que se supone que contribuye a la percepción del aroma a vainilla. El papel sensorial de los aldehídos fenólicos ha sido, y es, muy discutido, El siringaldehído y otros aldehídos fenólicos de la serie cinámica son muy poco odorantes, por lo que su contribución al aroma del vino debería ser nula; sin embargo, se ha encontrado21 que, en licores, el siringaldehído se puede transformar en vainillina y esto hace pensar que, si esta misma transformación ocurre en el vino, su contribución al aroma, aunque indirecta, puede ser importante. También se ha señalado un elevado grado de sinergismo entre aldehídos fenólicos y ácidos vainíllico, sinápico y ferúlico.22
El descriptor vainillina aparece frecuentemente asociado a sustancias que no poseen ese olor. Así se ha encontrado que niveles de 10 mg L-1 de furfural y 1 mg L-1 de cis-whiskylactona producen aromas a vainilla, caramelo y madera; curiosamente al incrementar los niveles de furfural se debilita el olor a madera mientras que aumenta el olor a vainilla y caramelo.16
Por otra parte, la vainillina se ha asociado al descriptor vainilla, pero más fuertemente a los descriptores café y chocolate negro, y ahumado.23 También se han encontrado vinos con este descriptor y cuyo contenido en vainillina estaba por debajo de su umbral de detección.17 Lo contrario también se ha publicado24 y se ha sugerido que la vainillina no ejerce un papel importante en el aroma de los vinos envejecidos en barrica.
Los catadores, frecuentemente, describen en los vinos envejecidos en barricas nuevas el aroma a vainilla, mientras que no lo hacen en vinos envejecidos en barricas usadas. En estas últimas predominaban los descriptores de aromas a caballo, herbáceos o farmacéuticos a pesar de que su contenido en etilfenoles no era alto.9
La lectura del papel sensorial que pueden desempeñar en el vino criado en barrica los diferentes compuestos reseñados conduce a pensar en el carácter multivariante de la percepción y en las correlaciones positivas y negativas entre compuestos. Algunas de ellas han quedado ya demostradas,4 pero las interacciones entre muchos compuestos sigue siendo una tarea pendiente.
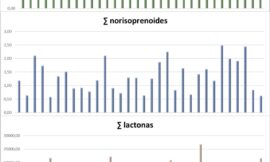
También llaman la atención ciertas ausencias. En la descripción del aroma de muchos vinos aparece el aroma a melocotón y ese olor no corresponde a ninguno de los compuestos citados anteriormente, sino a otras lactonas que aparecen en el vino, concretamente las γ- y δ-lactonas. Tampoco aparecen los productos derivados de los norisoprenoides β-ionona y β-damascenona, con olor a violeta y manzana asada,25 ni ciertas enolonas con aromas a caramelo, o de importancia sensorial bien conocida como el sotolón.26 Por esta razón en uno de nuestros trabajos abordamos el estudio de la importancia de los γ- y δ-lactonas y sus efectos combinados.2
Agradecimientos
Los datos presentados en este estudio, y su interpretación se han obtenido en el Laboratorio de Análisis del Aroma y Enología de la Universidad de Zaragoza en un trabajo en colaboración con la Estación de Viticultura y Enología de la Comunidad Foral de Navarra y con la Bodega Príncipe de Viana (51 y 52). Ha sido financiado por la Caja Rural de Navarra. Constituye, en parte, un capítulo de la Tesis Doctoral de Idoya Jarauta,2 tesis codirigida por Vicente Ferreira y el firmante.
Nota: Siga leyendo la segunda parte de este artículo en ACENOLOGIA: Estudio comparativo del perfil volátil del vino tinto durante su crianza en barricas de roble
Bibliografía
1. Aznar M.: «Jerarquización, identificación y determinación cuantitativa de los odorantes más importantes de los vinos de crianza españoles. Construcción de modelos quimiométricos para la predicción de los descriptores sensoriales a partir de la composición química», Tesis Doctoral, Facultad de Ciencias, Universidad de Zaragoza, 2002.
2. Jarauta I.: «Estudio analítico de fenómenos concurrentes en la generación del aroma durante la crianza del vino en barricas de roble con diferentes grados de uso. Nuevos métodos de análisis de importantes aromas y caracterización de su papel sensorial», Tesis Doctoral, Facultad de Ciencias, Universidad de Zaragoza, 2004.
3. Chatonnet P.: «Volatile and odoriferous compounds in barrel-aged. Wines: Impact of cooperage techniques and aging conditions», en: Chemistry of wine of wine flavor, cap. 14, 1998: 180-207.
4. Cutzach I. et al.: «Identification of Volatile Compounds with a Toasty Aroma in Heated Oak Used in Barrelmaking», Journal of Agricultural and Food Chemistry 1997; 45 (6): 2217-2224. 5. Cutzach I. et al.: «Identifying new volatile compounds in toasted oak», Journal of Agricultural and Food Chemistry 1999; 47 (4): 1663-1667.
6. Boidron J.N., Chatonnet P., Pons M.: «Influence du bois sur certaines substances odorantes des vins», Connaissance de la vigne et du vin 1988; 22 (4): 275-293.
7. Towey J.P.; Waterhouse A.L.: «The Extraction of Volatile Compounds From French and American Oak Barrels in Chardonnay During Three Successive Vintages», American Journal of Enology and Viticulture 1996; 47 (2): 163-172.
8. Pérez-Prieto L.J. et al.: «Maturing wines in oak barrels. Effects of origin, volume, and age of the barrel on the wine volatile composition», Journal of Agricultural and Food Chemistry 2002; 50 (11): 3272-6.
9. Aznar M. et al.: «Prediction of aged red wine aroma properties from aroma chemical composition. Partial least squares regression models», Journal of Agricultural and Food Chemistry 2003; 51 (9): 2700-2707.
10. Schreier P., Drawert F.: («Investigation of volatile components in wine by gas chromatography and mass spectrometry. I Nonpolar compounds of wine aroma»), «Gaschromatographisch-massenspektrometrische Untersuchung fluechtiger Inhaltsstoffe des Weines. I Unpolare Verbindungen des Weinaromas», Zeitschrift fuer Lebensmittel Untersuchung und Forschung 1974; 154: 273-278.
11. Rapp A., Mandery H.: «Wine aroma», Experientia 1986; 42: 873-884.
12. Díaz-Plaza E.M. et al.: «Influence of oak wood on the aromatic composition and quality of wines with different tannin contents», Journal of Agricultural and Food Chemistry 2002; 50 (9): 2622-2626.
13. Garde T., Rodriguez Mozaz S., Ancín Azpilicueta C.: «Volatile composition of aged wine in used barrels of French oak and of American oak», Food Research International 2002; 35 (7): 603-610.
14. Chatonnet P. et al.: «The origin of ethylphenols in wines», Journal of the Science of Food and Agriculture 1992; 60 (2): 165-178.
15. Chatonnet P., Dubourdieu D., Boidron J.N.: «Incidence des conditions de fermentation et d’élevage des vins blancs secs en barriques sur leur composition en substances cédées par le bois de chêne», Sciences des Aliments 1992a; 12: 665-685.
16. Reazin G.: «Chemical mechanisms of whiskey maturation», American Journal of Enology and Viticulture1981; 32: 283-289.
17. Díaz-Plaza E.M. et al.: «Influence of oak wood on the aromatic composition and quality of wines with different tannin contents», Journal of Agricultural and Food Chemistry 2002; 50 (9): 2622-2626.
18. Spillman P.J., Sefton P.G.: «Accumulation of volatile oak compounds in a model wine stored in American and Limousin barrels», Australian Journal of Grape and Wine Research 1998b; 4: 67-73.
19. Spillman P.J. et al.: «Formation and degradation of furfuryl alcohol, 5-methylfurfuryl alcohol, vanillyl alcohol, and their ethyl ethers in barrel-aged wines», Journal of Agricultural and Food Chemistry 1998; 46 (2): 657-663.
20. Chatonnet P., Boidron J.N., Pons M.: «Maturation of red wines in oak barrels: evolution of some volatile compounds and their aromatic impact», Sciences des Aliments 1990; 10: 565-587.
21. Puech J.L.: «Extraction of Phenolic Compounds from Oak Wood in Model Soluctions and Evolucion of Aromatic Aldehydes in Wines Aged in Oak Barrels», American Journal of Enolgy and Viticulture 1987; 38: 236-238.
22. Maga J.A.: «Flavor contribution of wood in alcoholic beverages», Progress in Flavour Research, 1984.
23. Spillman P.J. et al.: «Accumulation of Vanillin During Barrel-Aging of White, Red, and Model Wines», Journal of Agricultural and Food Chemistry 1997; 45 (7): 2584-2589.
24. Dubois P.: «Apports du fut de chêne neuf a l’arôme des vins», Revue des Oenologues 1989; 120: 19-24.
25. López R.F., Hernández P., Cacho J.: «Identification of impact odorants of young red wines made whit Merlot, Cabernet Sauvignon and Granche grape varieties: a comparative study», Journal of the Science of Food and Agriculture 1999; 79: 1461-1467.
26. Etiévant P.X.: «Wine», en: Volatile compounds in foods and beverages, 1991: 483-546.
27. Ortega C. et al.: «Fast analysis of important wine volatile compounds: Development and validation of a new method based on gas chromatographic-flame ionisation detection analysis of dichloromethane microextracts», Journal of Chromatography A 2001; 923 (1-2): 205-214.
28. López R. et al.: «Determination of minor and trace volatile compounds in wine by solid-phase extraction and gas chromatography with mass spectrometric detection», Journal of Chromatography A 2002; 966 (1-2): 167-177.
29. Ferreira V., Jarauta I., López R., Cacho J.: «Quantitative determination of sotolon, maltol, and free furaneol in wine by solid-phase extraction and gas chromatography-ion.trap mass spectrometry», Journal of Chromatography A 2003; 1010: 95-103.
30, Ferreira V., Jarauta I., Ortega L., Cacho J: «Simple strategy for optimization of solid-phase extraction procedures through the use of solid-liquid distribution coefficients. Application to the determination of aliphatic lactones in wine», Journal of Chromatography A 2004; 1025: 147-156.
31. Lopez R. et al.: «Analysis of the aroma intensities of volatile compounds released from mild acid hydrolysates of odourless precursors extracted from Tempranillo and Grenache grapes using gas chromatography-olfactometry», Food Chemistry 2004; 88 (1): 95-103.
32. Hanna Peleg, M.N., Uri Zehavi, Russell L. Rouseff, Steven Nagy: «Pathways of 4-vinylguaiacol formation from ferulic acid in model solutions of orange juice», Journal of Agricultural and Food Chemistry 1992; 40 (5): 764-767.
33. Romero DA: «Bacteria as potential sources of flavor metabolites», Food- Technology 1992; 46 (11): 122, 124-126.
34. Bertrand AR, G., Pripis-Nicolau L: «Sensory evaluation of consequences of malolactic fermentation for white in barrels. Bulletin de l’OIV 2000; 73 (831/832): 313-321.
35. Brunati MM, F Bertolini, C Gandolfi, R Daffonchio, D Molinari F: «Biotransformation fo cinnamic and ferulic acid with actinomycetes», Enzyme and microbial technology 2004; 34 (1): 3-9.
36. Miller DP et al.: «The Content of Phenolic-Acid and Aldehyde Flavor Components of White Oak as Affected by Site and Species», American Journal of Enology and Viticulture 1992; 43 (4): 333-338.
37. Pollnitz AP, K.H. Pardon, M.A. Sefton: «Quantitative analysis of 4-ethylphenol and 4-ethylguaiacol in red wine», Journal of Chromatography A 2000; 874 (1): 101-109.
38. Muller CJ, R.E. Kepner, A.D. Webb: «Lactones in wines – a review», American Journal of Enology and Viticulture 1973; 24 (1): 5-9.
39. Garde T, D. Torrea, C. Ancin: «Accumulation of volatile compounds during ageing of two red wines with different composition», Journal of Food Engineering 2004; 65 (3): 349-356.
40, Cutzach I. et al.: «Study in aroma of sweet natural non Muscat wines. II. Quantitative analysis of volatile compounds taking part in aroma of sweet natural wines during ageing», Journal International des Sciences de la Vigne et du Vin 1998; 32 (4): 211-221.
41. Moreno JA et al.: «Aroma compounds as markers of the changes in sherry wines subjected to biological ageing. Food Control» (en prensa).
42. Van Gemert LJ: Compilations of Odour Threshold Values in Air and Water. 2003, Boelens Aroma Chemical Information Service.
43. Ferreira V, Cacho J: «Quantitative determination of the odorants of young red wines from different grape varieties», Journal of the Science of Food and Agriculture 2000; 80: 1659-1667.
44. Guth H: «Quantification and sensory studies of character impact odorants of different white wine varieties. Journal of Agricultural and Food Chemistry 1997; 45(8): 3027-3032.
45. Cutzach I, P. Chatonnet, D. Dubourdieu: «Influence of Storage-Conditions on the Formation of Some Volatile Compounds in White Fortified Wines (Vins Doux Naturels) During the Aging Process», Journal of Agricultural and Food Chemistry 2000; 48 (6): 2340-2345.
46. Nakamura SC, EA, Ough CS, Totsuka A: «Quantitative analysis of g-nonalactona in wines and its threshold determination», Journal of Food Science 1988. 53: p. 1243-1244.
47. Cullere L, Cacho J, Ferreira V: «Gas Chromatography-Olfactometry and Chemical Quantitative Study of the Aroma of Six Premium Quality Spanish Aged Red Wines», Journal of Agricultural and Food Chemistry 2004; 52 (6): 1653-1660.
48. López R et al.: «Determination of minor and trace volatile compounds in wine by solid-phase extraction and gas chromatography with mass spectrometric detection», Journal of Chromatography A 2002; 966 (1-2): 167-177.
49. Masuda M et al.: «Identification of 4,5-dimethyl-3-hydroxy-2(5H)-furanone (Sotolon) and ethyl 9-hydroxynonanoate in botrytised wine and evaluation of the roles of compounds characteristic of it», Agricultural and Biological Chemistry 1984; 48 (11): 2707-2710.
50. http://www.leffingwell.com/index.htm.
51. Jarauta I, Cacho J, Ferreira V: «Concurrent Phenomena Contributing to the Formation of the Aroma of Wine during Aging in Oak Wood: An Analytical Study», Journal of Agricultural and Food Chemistry 2005; 53 (10): 4166-4177.
52. Ferreira V, Jarauta I, Cacho J: «Physicochemical Model to Interpret the Kinetics of Aroma Extraction during Wine Aging in Wood. Model Limitations Suggest the Necessary Existence of Biochemical Processes», Journal of Agricultural and Food Chemistry 2006; 54: 3047-3054.