En las últimas décadas, los hábitos de consumo de la población han evolucionado desde la prioridad en el pasado de cubrir la demanda de nutrientes hasta día de hoy en que, con sus necesidades nutricionales, el consumidor demanda prioritariamente alimentos sanos y especialmente seguros. La enología no escapa de esta tendencia, de manera que ya se utilizan instrumentos como el análisis de peligros y puntos de control críticos (APPCC) para prevenir la presencia de elementos que puedan ser perjudiciales para el consumidor.1
El primer objetivo de la seguridad alimentaria es evitar los microorganismos patógenos que en el caso del vino no suponen ningún riesgo. Son, por tanto, los peligros químicos los que se deben tener en cuenta. Entre los compuestos químicos que podemos encontrar en el vino y que pueden suponer un riesgo para el consumidor destaca la presencia de azufre. En este artículo se ha realizado una revisión de las distintas fuentes de azufre que podemos encontrar en el vino, así como las principales alternativas que se conocen hoy en día.
Presencia de azufre en vino: los pesticidas
 El azufre es uno de los elementos químicos más usado y controvertido en enología. Su incorporación tiene varias finalidades. Por un lado, se utiliza en la viña como protector frente al crecimiento de hongos fitopatógenos, especialmente oídio y mildiu. El azufre forma parte de numerosos pesticidas y fungicidas autorizados en la Unión Europea, aunque poco se sabe del potencial de estas moléculas para romperse y liberar azufre.2
El azufre es uno de los elementos químicos más usado y controvertido en enología. Su incorporación tiene varias finalidades. Por un lado, se utiliza en la viña como protector frente al crecimiento de hongos fitopatógenos, especialmente oídio y mildiu. El azufre forma parte de numerosos pesticidas y fungicidas autorizados en la Unión Europea, aunque poco se sabe del potencial de estas moléculas para romperse y liberar azufre.2
El azufre usado en viticultura puede acabar en el vino, aunque siempre en menor cantidad dependiendo del proceso de vinificación utilizado y de la concentración inicial en la uva.3 El uso de pesticidas o herbicidas es seguro siempre que se usen en las condiciones adecuadas y correctas siguiendo las buenas prácticas agrícolas y no se supere el limite máximo de residuos (LMR).4 En caso contrario, si el uso es excesivo quedan residuos de compuestos químicos en la uva que pasarán al vino. Por esa razón, en la práctica resulta mucho más útil y seguro utilizar métodos preventivos para mantener la calidad higiénica de la vid y, por tanto, de la uva.
Se han estudiado diversas prácticas enológicas por su capacidad para eliminar o bien disminuir la cantidad de pesticidas en el vino. Durante el prensado de la uva parte de los pesticidas permanecen en la parte sólida y solo en función de sus características químicas pasarán al mosto. La fermentación disminuye también la cantidad de ciertos pesticidas mientras que otros pueden llegar a eliminarse completamente.5 Finalmente, las etapas de clarificación son importantes para disminuir la presencia de estos compuestos en vino. Algunos de los más comunes como bentonita, charcoal o polivinilpirrolidona han mostrado cierta capacidad para disminuir la concentración de residuos de pesticidas siendo el charcoal el que ha mostrado mayor eficiencia llegando a eliminarlos casi totalmente.5
Entre los métodos menos agresivos propuestos destacan incrementar las defensas naturales de la planta mediante las llamadas fitoalexinas. En la vid, las fitoalexinas son bien conocidas, pertenecen a la familia de los estilbenos siendo la más conocida el resveratrol.
El resveratrol responde al ataque de hongos, la radiación UV, el ozono y la presencia de metales.6
v
El dióxido de azufre
El dióxido de azufre (SO2) se utiliza como conservante desde el siglo XVIII. Se usa como aditivo en el vino por su actividad antioxidante, especialmente sobre la polifenoloxidasa pero también por su actividad antimicrobiana sobre levaduras, bacterias lácticas y bacterias del ácido acético. Además, el dióxido de azufre influye sobre las características organolépticas del vino al evitar la formación de defectos en el vino ya que neutraliza compuestos volátiles. Por tanto, se usa tanto para evitar el crecimiento de microorganismos indeseables en el vino como en operaciones prefermentativas para evitar las oxidaciones enzimática y no enzimática del mosto.
En el vino, el SO2 se encuentra en equilibrio entre sus distintas formas libres, que son activas, y sus formas combinadas, que son inactivas respecto de las propiedades descritas. Desde el punto de vista de seguridad alimentaria el SO2 debe ser utilizado en la menor cantidad posible, tanto por razones de salud del consumidor como para evitar la formación de moléculas como mercaptanos o hidrosulfato, que constituyen defectos organolépticos del vino.7
«Los sulfitos provocan efectos adversos en determinados consumidores y siempre en función de la dosis. La sintomatología es variable y depende de la sensibilidad de cada consumidor.»
Una de las formas libres, los sulfitos, resultante de la adición de SO2 al vino, producen efectos adversos en determinados consumidores, siempre en función de la dosis.4,8 A pesar de que no se trata de una alergia verdadera, los sulfitos pueden producir en personas sensibles una sintomatología de alergia como enrojecimiento de la cara, dolor de cabeza, picor de garganta, dificultades respiratorias e incluso, en algunos casos, náuseas y vómitos. Los datos indican que un 1% de la población es sensible a los sulfitos mientras que entre la población asmática este porcentaje aumenta hasta el 5%.4 La dosis necesaria para desencadenar dicha sintomatología es variable ya que depende de la sensibilidad del consumidor. En todo caso, en población asmática la reacción puede ser grave; está descrito en la bibliografía la posibilidad que, en determinadas condiciones excepcionales, los sulfitos activen protooncogenes, inactiven genes supresores de tumores y puedan tener un papel en la patogénesis de ciertos cánceres de pulmón asociados a SO2.7,9
| Sulfitos y legislación
En Europa, el dióxido de azufre y los sulfitos están autorizados en distintas formas, y sus códigos asignados van del E-220 al E-228 (dióxido de azufre, sulfito sódico, hidrogeno sulfito sódico, metabisulfito sódico, metabisulfito potásico, sulfito cálcico, hidrogeno sulfito cálcico, y hidrogeno sulfito potásico).10 La legislación indica las cantidades máximas de sulfito que se pueden usar en vino que van des de 160 mg/L en vino tinto y 210 mg/L en vinos blancos y rosados.11 Las recomendaciones de la Organización Internacional de la Viña y el Vino (OIV) van desde 150 mg/L en vinos tintos a 400 mg/L en vinos dulces.12 La Agencia Europea de Seguridad Alimentaria (EFSA) ha reevaluado recientemente la seguridad del uso de sulfitos como aditivos.13 En resumen, a pesar de que se indica la necesidad de aumentar la base de datos sobre estos aditivos, el NOAEL (acrónimo en inglés de no observed adverse effect level, es decir, dosis que no produce efectos adversos) se mantiene en 70 mg/kg peso corporal/día, y la ingesta diaria admisible (IDA) en 0,7 mg/kg peso corporal/día. La estimación de la exposición a los sulfitos es superior a la IDA en gran parte de la población, siendo el vino la principal fuente de sulfitos en la población adulta. Además, y desde 2005, es de obligado cumplimiento el indicar en el etiquetado la presencia de sulfitos en vino cuando la cantidad sea superior a 10 mg/L. A pesar de que actualmente el uso de SO2 no tiene una alternativa viable,7 es indispensable seguir trabajando para encontrarla, tanto por razones de salud como por la exigencia del propio mercado y las demandas del consumidor. |
Las alternativas al SO2
Como se ha descrito anteriormente, la función del SO2 no es solamente controlar el crecimiento y fermentación de microorganismos no deseados, sino también evitar procesos oxidativos debidos, por ejemplo, a la actividad de la enzima polifenol oxidasa (PPO) durante la elaboración, siendo añadido al mosto y también al vino tras finalizar la fermentación maloláctica.7,14
Debido a las restricciones en la elaboración de los vinos ecológicos, y también los llamados naturales, puesto que deben contener una menor concentración de SO2 total (150 mg/L para vinos tintos y 100 mg/L para blancos y rosados),15 son más propensos a sufrir una degradación oxidativa.16 Por ello, se necesitan alternativas que consigan el mismo efecto antioxidante y antimicrobiano que el SO2, y que aseguren que el producto final es estable microbiológicamente, además de que esté protegido frente a la oxidación, sin perder calidad y manteniendo las propiedades organolépticas del vino.17
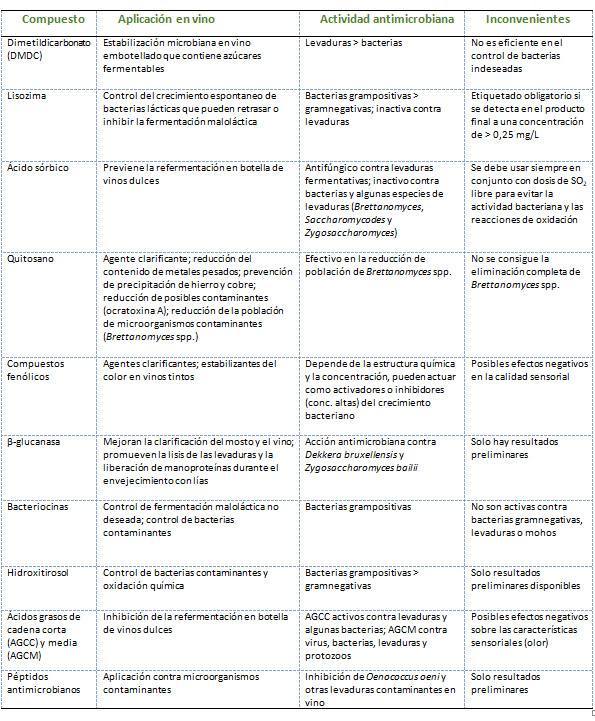
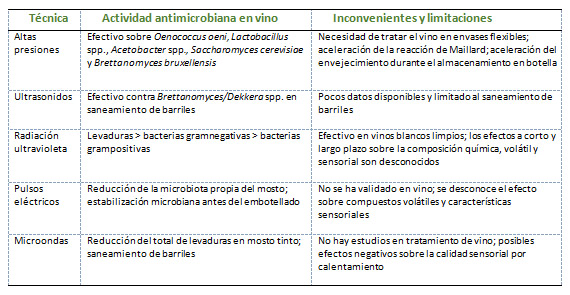
Para sustituir el SO2 se han propuesto diferentes compuestos químicos como la lisozima, la β-glucanasa, el dimetildicarbonato (DMDC) o el ácido sórbico,17 cuyo uso está permitido en vinos, aunque, siguiendo el Reglamento (CE) 203/2012,15 no lo está en la producción de vinos ecológicos. Por otro lado, se están estudiando otras alternativas mediante métodos químicos (tabla 1) y físicos (tabla 2). Entre ellas destacan el quitosano y los compuestos fenólicos.
Quitosano
El quitosano es un heteropolisacárido derivado de la quitina por desacetilación, con una reconocida actividad antimicrobiana.18 Es biodegradable, biocompatible y no tóxico.17,19 Aunque su mecanismo de acción no se ha dilucidado, la principal hipótesis se basa en una alteración de la permeabilidad de la membrana bacteriana, que resulta en la filtración de los componentes intracelulares al exterior, causando la muerte celular.
Diferentes estudios han constatado que bajas dosis de quitosano (0,04-0,5 g/L) son capaces de inhibir el crecimiento de Brettanomyces bruxellensis, reduciendo sus niveles de población en pruebas de laboratorio. Sin embargo, no se ha conseguido su eliminación completa, ya que finalmente las poblaciones de B. bruxellensis alcanzaron niveles mayores de población al cabo de un tiempo de haber finalizado el tratamiento con quitosano.20-22
Por lo tanto, el quitosano debería considerarse como complemento al SO2, pero no un sustituto completo para reducir las poblaciones de B. bruxellensis en vino, aunque sí puede ser una opción para conseguir vinos con menos contenido en SO2. Además, Ferreira et al.20 observaron que al finalizar del experimento la concentración de quitosano libre era indetectable, por lo que sugirieron que este reacciona con otras moléculas presentes de forma natural en el vino. También observaron que el quitosano afecta al color del vino, disminuyendo su intensidad, pero aumentando el tono. Respecto de su acción antimicrobiana, un estudio reciente demuestra la efectividad del quitosano para reducir las poblaciones de bacterias acéticas y su actividad metabólica en el vino.23
Compuestos fenólicos
Los compuestos fenólicos se encuentran de forma natural como constituyentes de la uva y el vino. Dentro de los compuestos fenólicos existen moléculas con diversas estructuras químicas, incluyendo el ácido hidroxibenzoico, ácidos hidroxicinámicos, estilbenos, alcoholes, flavanoles, antocianinas y taninos.
Estos compuestos son responsables de algunas de las características organolépticas del vino, como el color y la astringencia, y su concentración depende de diversos factores relacionados con la uva (variedad, clima, calidad de la vendimia, etc.), además de las prácticas enológicas. Por ello, su contenido en vino suele oscilar entre 150-400 mg/L en vinos blancos y 900-1400 mg/L en tintos.24 Varios estudios sugieren su aplicación como potenciadores y como inhibidores del crecimiento bacteriano.25-27 Por ejemplo, el ácido gálico y la catequina, a las concentraciones que se encuentran en vino, son capaces de estimular el crecimiento de Lactobacillus hilgardii, debido a su capacidad para metabolizar estos compuestos durante la fase de crecimiento. Además, también pueden afectar al metabolismo bacteriano ya que favorecen el uso de azúcares y ácido málico.25
«Los extractos polifenólicos (que contienen principalmente ácidos fenólicos) son más eficaces contra bacterias que contra levaduras.»
Por otra parte, a concentraciones más altas, estos mismos compuestos pueden tener un efecto negativo en las bacterias, dependiendo del microorganismo, siendo, por ejemplo, más sensible Oenococcus oeni que L. hilgardii.26 Se conoce su mecanismo de acción exacto, aunque algunos autores sugieren que los compuestos fenólicos pueden modificar la permeabilidad de la membrana bacteriana y alterar la composición de los ácidos grasos.28 De este modo, los extractos polifenólicos (que contienen principalmente ácidos fenólicos) son más eficaces contra bacterias que contra levaduras.24 Sin embargo, la eficacia de los compuestos fenólicos como agentes antimicrobianos en vino depende tanto de la estructura del compuesto como de la dosis aplicada. En general, este efecto antimicrobiano suele aparecer en dosis más altas de las que se encontrarían habitualmente en un vino.24 Además, se deberían tener en cuenta posibles consecuencias negativas del uso de compuestos fenólicos a altas concentraciones ya que, por ejemplo, una concentración elevada de taninos puede tener un efecto negativo sobre las características sensoriales en el vino tinto.17
Por otro lado, también están surgiendo nuevos productos, como Vineatrol® (Actichem S.A.; Montauban, Francia), basado en un extracto de los sarmientos de la vid, o Geolife® (Bioma S.A.; Quartino, Suiza), que es un concentrado de compuestos fenólicos y antocianos. Según Raposo, et al.,29 el uso del Vineatrol® con un 30% de estilbenos es capaz de garantizar la calidad en vinos tintos, con mayor intensidad de color y un buen perfil fenólico. El uso de este producto supondría la producción de vinos tintos con un valor añadido, bajas concentraciones de SO2 y un alto contenido en estilbenos, además de contribuir a la sostenibilidad de la industria vitivinícola al revalorizar un subproducto como son los sarmientos.
Conclusiones
Actualmente, el consumidor demanda productos más naturales con menor uso de sustancias químicas y que sean más respetuosos con el medio ambiente. La elaboración de vinos ecológicos, y naturales, va en esta dirección, aunque la disminución o la no utilización de algunos compuestos químicos pueden dar lugar a problemas en el producto final. El uso de productos derivados de azufre para favorecer la conservación del vino tanto en la vid como en el mosto y vino puede ser a largo plazo perjudicial para el consumidor, por lo que el estudio de alternativas más naturales y sostenibles puede ser una buena opción para dar respuesta a las demandas del consumidor.
Bibliografía
1. Benito S. The management of compounds that influence human health in modern winemaking from an HACCP point of view. Fermentation 2019; 5: 33-53.
2. Smith M.E., Bekker M.Z., Smith P.A., Wilkes E.N. Sources of volatile sulfur compounds in wine. Australian Journal of Grape and Wine Research, 2015; 21: 705-12.
3. Cabras P., Angioni A. Pesticide residues in grapes, wine, and their processing products. Journal of Agricultural and Food Chemistry 2000; 48; 967-73.
4. Pozo-Bayón M.A., Monagas M., Bartolomé B., Moreno-Arribas M.V. (2012). Wine features related to safety and consumer health: an integrated perspective. Critical Reviews in Food Science and Nutrition 2012; 52: 31-54.
5. Cabras P., Garau V.L., Melis M., Pirisi F.M., Tuberoso C.I.G. The effect of clarifying substances on organophosphorous insecticide residues in wine. Journal of WineResearch 1995; 6: 201-5.
6. Jeandet P., Douillet-Breuil A.-C., Bessis R., Debord S., Sbaghi M., Adrian M. Phytoalexins from the Vitaceae: biosynthesis, phytoalexin gene expression in transgenic plants, antifungal activity, and metabolism. Journal of Agricultural and Food Chemistry 2002; 50: 2731−41.
7. Guerrero R.F., Cantos-Villar E. Demonstrating the efficiency of sulphur dioxide replacements in wine: a parameter review. Food Science and Technology 2015; 42: 27-43.
8. Santos M.C., Nunes C., Saraiva J.A., Coimbra M.A. (2012). Chemical and physical methodologies for the replacement/reduction of sulfur dioxide use during winemaking: review of their potentialities and limitations. European Food Research and Technology 2012; 234: 1-12.
9. Qin G., Meng Z. Effects of sulfur dioxide derivatives on expression of oncogenes and tumor suppressor genes in human bronchial epithelial cells. Food and Chemical Toxicology 2009; 47: 734-44.
10. European Comission. Commission regulation (EU) No 1129/2011 of 11 November 2011 amending Annex II to Regulation (EC) No 1333/2008 of the European Parliament and of the Council by establishing a Union list of food additives. Official Journal of the European Communities 2011; L 295/1.
11. European Comission. Council regulation (EC) nº 1493/1999 of 17 de may 1999 on the common organization of the market in wine. Official Journal of the European Communities 1991; L 179/1.
12. OIV. International Code of Oenological Practices. Maximum acceptable limits. OIV Code Sheet 2015; 01.
13. EFSA. Scientific Opinion on the re-evaluation of sulfurdioxide (E 220), sodium sulfite (E 221), sodium bisulfite (E 222), sodium metabisulfite (E 223), potassium metabisulfite (E 224), calcium sulfite (E 226), calcium bisulfite (E 227) and potassium bisulfite (E 228) as food additives. EFSA Journal 2016; 14: 4438.
14. Ribéreau‐Gayon P., Dubourdieu D., Donèche B., Lonvaud A. The use of sulfur dioxide in must and wine treatment. En: P. Ribéreau-Gayon, D. Dubourdieu, B. Donèche, A. Lonvaud (eds.). Handbook of Enology. Vol. 1: The Microbiology of Wine and Vinifications. 2ª ed. Wiley, 2006: p. 193-221.
15. European Comission. Commission implementing regulation (EU) No 203/2012 of 8 March 2012amending Regulation (EC) No 889/2008 laying down detailed rules for theimplementation of Council Regulation (EC) No 834/2007, as regards detailed rules onorganic wine. Official Journal of the European Communities 2012; L42-27.
16. Lagunero T., Aznar M., Ferreira A. Alternatives for avoiding degradation in ecological wine. Italian Journal of Food Science 2011; 23: 55-8.
17. Lisanti M.T., Blaiotta G., Nioi C., Moio L. Alternative methods to SO2 for microbiological stabilization of wine. Comprehensive Reviews in Food Science and Food Safety 2019; 18: 455-79.
18. Bağder Elmacı S., Gülgör G., Tokatlı M., Erten H., İşci A., Özçelik F. (2015). Effectiveness of chitosan against wine-related microorganisms. Antonie van Leeuwenhoek 2015; 107: 675-86.
19. Raafat D., Sahl H.-G. Chitosan and its antimicrobial potential: a critical literature survey. Microbial Biotechnology 2009; 2: 186-201.
20. Ferreira D., Moreira D., Costa E.M., Silva S., Pintado M.M., Couto J.A. The antimicrobial action of chitosan against the wine spoilage yeast Brettanomyces/Dekkera. Journal of Chitin and Chitosan Science 2013; 1: 240-45.
21. Petrova B., Cartwright Z.M., Edwards C.G. Effectiveness of chitosan preparations against Brettanomyces bruxellensis grown in culture media and red wines. OENO One 2016; 50: 49.
22. Taillandier P., Joannis-Cassan C., Jentzer J.-B., Gautier S., Sieczkowski N., Granes D., Brandam C. Effect of a fungal chitosan preparation on Brettanomyces bruxellensis, a wine contaminant. Journal of Applied Microbiology 2015; 118: 123-31.
23. Valera M.J., Sainz F., Mas A., Torija M.J. Effect of chitosan and SO2 on viability of Acetobacter strains in wine. International Journal of Food Microbiology 2017; 246: 1-4.
24. García-Ruiz A., Bartolomé B., Martínez-Rodríguez A.J., Pueyo E., Martín-Álvarez P. J., Moreno-Arribas M.V. Potential of phenolic compounds for controlling lactic acid bacteria growth in wine. Food Control 2008; 19: 835-41.
25. Alberto M.R., Farías M.E., Manca de Nadra M.C. Effect of gallic acid and catechin on Lactobacillus hilgardii 5w growth and metabolism of organic compounds. Journal of Agricultural and Food Chemistry, 2001; 49: 4359-63.
26. Campos F.M., Couto J.A., Hogg T.A. Influence of phenolic acids on growth and inactivation of Oenococcus oeni and Lactobacillus hilgardii. Journal of Applied Microbiology 2003; 94: 167-74.
27. Reguant C., Bordons A., Arola L., Rozes N. Influence of phenolic compounds on the physiology of OEnococcus oeni from wine. Journal of Applied Microbiology 2000; 88: 1065-71.
28. Rozès N., Peres C. Effects of phenolic compounds on the growth and the fatty acid composition of Lactobacillus plantarum. Applied Microbiology and Biotechnology 1998; 49: 108-11.
29. Raposo R., Chinnici F., Ruiz-Moreno M.J., Puertas B., Cuevas F.J., Carbú M., Guerrero R.F., Ortiz-Somovilla V., Moreno-Rojas J.M., Cantos-Villar E. Sulfur free red wines through the use of grapevine shoots: Impact on the wine quality. Food Chemistry 2018; 243: 453-60.
Bibliografía recomendada
.Kuchen B., Maturano Y.P., Mestre M.V., Combina M., Toro M.E., Vázquez F. Selection of native non-Saccharomyces yeasts with biocontrol activity against spoilage yeasts in order to produce healthy regional wines. Fermentation 2019; 5: 60.
.Raposo R., Ruiz-Moreno M.J., Garde-Cerdán T., Puertas B., Moreno-Rojas J.M., Gonzalo-Diago A., Guerrero R.F., Ortiz V., Cantos-Villar E. Effect of hydroxytyrosol on quality of sulfur dioxide-free red wine. Food Chemistry 2016; 192: 25-33.
.Raposo R., Ruiz-Moreno M.J., Garde-Cerdán T., Puertas B., Moreno-Rojas J.M., Zafrilla P., Cantos-Villar E. Replacement of sulfur dioxide by hydroxytyrosol in white wine: Influence on both quality parameters and sensory. LWT – Food Science and Technology 2016; 65: 214-21.
.Ruiz-Moreno M.J., Raposo R., Puertas B., Cuevas F.J., Chinnici F., Moreno-Rojas J.M., Cantos-Villar E. Effect of a grapevine-shoot waste extract on red wine aromatic properties. Journal of the Science of Food and Agriculture 2018; 98: 5606-15.
.Yoo K.S., Ahn J.E., Han J.S., Seo E., Otgonbayar G.E., Han N.S. Antimicrobial treatment of grapes using sodium hypochlorite in winemaking and its effects on the chemical and sensory characteristics of wines. Journal of Microbiology and Biotechnology 2011; 21: 1243-9.