El oxígeno, como segundo compuesto mayoritario del aire presente en un 20,95%, tiene una estrecha relación con diferentes reacciones de oxidorreducción que acontecen a lo largo de todo el proceso de vinificación. Estos procesos oxidativos en algunos casos son deseados e incluso buscados, mientras que, en otras etapas, el oxígeno es el enemigo a combatir y por eso se hace imprescindible conocerlo. Debemos ser capaces de realizar una medición con las garantías suficientes como para que estas nos ofrezcan valores fiables y a su vez útiles. De la misma forma se hace necesario saber interpretar los valores que se obtienen cuando se realizan lecturas con los diferentes equipos disponibles en el mercado. Para poder comprender cómo funcionan los sistemas y el significado de las medidas es necesario que repasemos someramente algunas cuestiones.
El oxígeno en el vino
La mayoría de los fluidos están en equilibrio con los gases que les rodean, y en el caso de que cumplan la ley de Henry este equilibrio permite hablar de la solubilidad. La cuestión es que la simplificación de la ley de Henry establece que el equilibrio entre el gas disuelto en un líquido y la atmosfera gaseosa que le rodea depende de que ambos tengan la misma presión parcial de ese gas concreto, tanto en el líquido disuelto como en el gas que lo rodea y con el que está en equilibrio.
La presión parcial de un gas concreto se puede entender mejor si la tomamos como el porcentaje en volumen de ese gas concreto (oxígeno) aplicado a la presión a la que se encuentra la mezcla de gases (aire). Es decir, que si estamos a la presión atmosférica a nivel del mar (1013 mbar = 1013 hPa = 1 atm) y el oxígeno está presente en el aire en un 20,95%, su presión parcial será ese mismo porcentaje de la presión; pO2 =1,013 hPa x 0,2095 = 212,22 hPa. Con esto podemos entender que, cuando midamos el oxígeno disuelto (OD) en un líquido en equilibrio con el aire, aquel tendrá un contenido en oxígeno de 212,22 hPa. Para que esto sea cierto es necesario que el aire tenga su composición teórica, situación que no sucede cuando el aire no está seco, es decir tiene humedad relativa o lo que es lo mismo, hay vapor de agua en el aire modificando de esta manera la composición porcentual de los diferentes compuestos. ¿Cómo solventamos este contratiempo? Simplemente sustrayendo la cantidad de vapor de agua de la presión atmosférica del aire. Así, una vez corregida la presión total del aire (P atm – presión parcial del vapor de agua), podemos nuevamente aplicar el porcentaje habitual del oxígeno en su composición y conocer la verdadera presencia de oxígeno disuelto en un líquido en equilibrio con el aire que le rodea, cuando el aire no está seco. Como la presión parcial del vapor de agua depende a su vez de la temperatura, es muy importante saber a qué temperatura se realiza la medida para así poder a su vez realizar una corrección, además de otras que se verán mas adelante. Cuando tengamos que realizar la medida en otras unidades diferentes que definen la presencia de un gas disuelto en un líquido, es necesario conocer algunos detalles importantes. El resto de unidades más habituales para expresar el oxígeno disuelto son %O2 saturación, % aire-saturación, Torr y la concentración, que es la que más nos gusta en el sector porque es la más palpable para nuestros intereses, concentración expresada en masa por unidad de volumen, en mg/litro (ppm) y en algunos procesos, en microgramos por litro (µg/litro o ppb).
La unidad %O2 sat viene a expresar si el porcentaje (%) es el que tendría que tener de acuerdo al que tiene en el aire (es decir en un líquido en equilibrio con aire seco será 20,95%), mientras que si se mide en % air-sat es una medida relativa, si tiene todo el que tendría que tener con respecto al aire, es decir cuando esté en equilibrio con el aire seco, el 100%. Para poder medir en concentración se usa la solubilidad del gas en el agua, que a su vez es dependiente, y mucho, de la temperatura, y aquí nuevamente se necesita corregir la medida con la temperatura.
Por tanto, los dispositivos que miden oxígeno disuelto deberían tener compensación de la medida con la temperatura del fluido en el que estamos midiendo, así como corrección con la presión atmosférica en la que realizamos la medida. La mayoría de los dispositivos presentes en el mercado cumplen con estas dos premisas.
La necesidad y la importancia de la medida del OD en vinos
Para conocer de qué niveles de oxígeno estamos hablando cuando queremos realizar su medida en el proceso de vinificación, vamos a revisar lo que otros autores y nosotros hemos observado y comprobar que existen dos niveles diferentes de OD durante todo el proceso de vinificación. Coloquialmente se puede hablar de una medida realizada en partes por millón (ppm = mg/L) y otra que se debe realizar en tres órdenes de magnitud más bajos, en partes por billón (ppb = µg/L). Evidentemente ya podemos deducir que es posible que los equipos necesarios para cada caso sean diferentes.
Los trabajos realizados por Vidal et al. 1-3 y por Castellari et al. 4 pusieron de manifiesto que existen claramente los dos niveles de aportes de oxígeno anteriormente citados, dependiendo de las operaciones concretas a las que se somete el vino. Este punto se puede observar claramente en la figura 1: en azul, las operaciones en las que la incorporación de oxígeno es muy elevada, hasta saturación en algunas ocasiones, lo que recomienda expresar el nivel en OD en mg/litro. Mientras, existen otras operaciones en las que el nivel medio de incorporación de OD está por debajo de 1 mg/L y lo habitual es trabajar con µg/litro (fig. 1 en rojo). Otra fase del proceso en la que los niveles de OD son igualmente bajos es en la crianza del vino en madera, ya que el vino es un gran consumidor de oxígeno y los niveles de incorporación muy bajos. (Véase la figura 7, del artículo de este dossier Oxígeno y barrica. Estado actual del conocimiento.)
a)
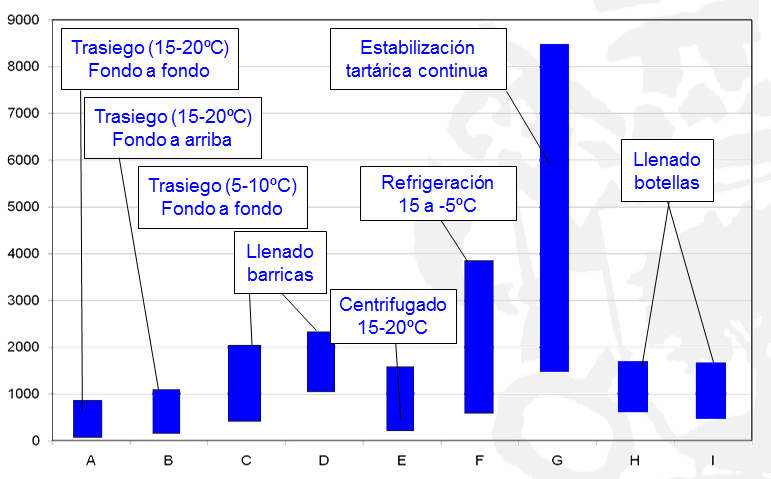
b)
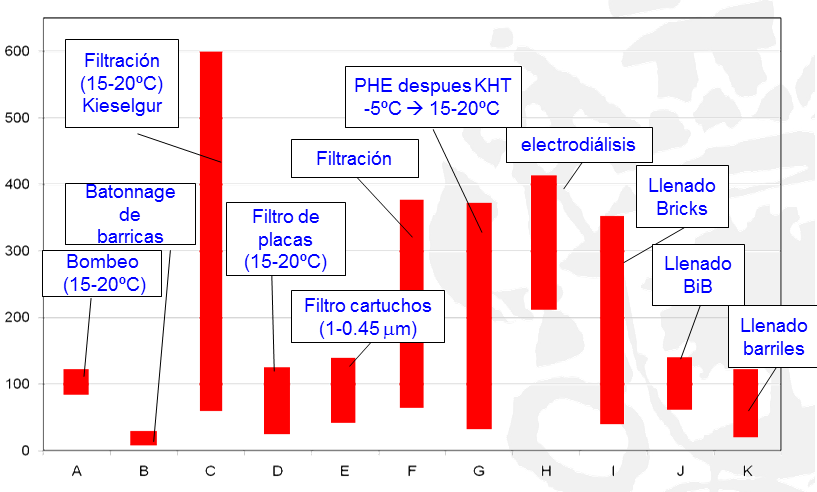
Los niveles de oxígeno disuelto en barricas resultan ser casi inexistentes a las dos semanas de permanencia del vino en la barrica (fig. 2). Estas medidas evidencian que los equipos con características suficientes para medir cantidades de mg/litro en procesos como trasiegos, centrifugado o llenado de diferentes sistemas (no deja de ser un movimiento de vino) y no digamos en procesos de enfriamiento de vinos (refrigeración o estabilización por frío), pueden no ser los más adecuados para medir niveles de µg/L habituales en otras operaciones como bombeos bien realizados, filtraciones o llenado de barricas, o incluso el batonnage de estas últimas, pero podrían valer. Lo que sí parece evidente es que los procesos de envejecimiento de vinos en barrica requieren equipos para medir concentraciones tan bajas como 10-30 µg/L, y para eso se hace necesario recurrir a sistemas de medida con límites de detección y resolución más bajos y con una precisión de la medida más alta. Hagamos ahora un repaso por los diferentes sistemas de medida de oxígeno que encontramos en el mercado, pensando siempre en su aplicación al sector enológico.
Sistemas de medida del oxígeno disuelto en líquidos
La medida del oxígeno disuelto en líquidos data de 1772 y era realizada mediante una gravimetría, posteriormente en 1888 el test de Winkler se utilizó para las medidas de oxígeno disuelto en agua, en 1924 los métodos manométricos se utilizaron para la medida del OD en sangre. A partir de la segunda mitad del siglo XX otros métodos se han venido utilizando: EPR (Electronic Paramagnetic Resonance), cromatografía de gases y aparece el primer sistema que posibilita la aplicación de una medida en proceso, el electrodo basado en la celda de Clark (1953). En 1968 aparecen las primeras sondas luminiscentes,5 aunque están basadas en los trabajos de Kautsky de 1939.6 A diferencia de los primeros sistemas, los dos últimos utilizan tecnologías (electroquímica y luminiscente) que permiten su aplicación en el ámbito industrial (fuera del laboratorio). Estas dos tecnologías son las que actualmente están mayoritariamente disponibles comercialmente, y en las que vamos a basar nuestro análisis.
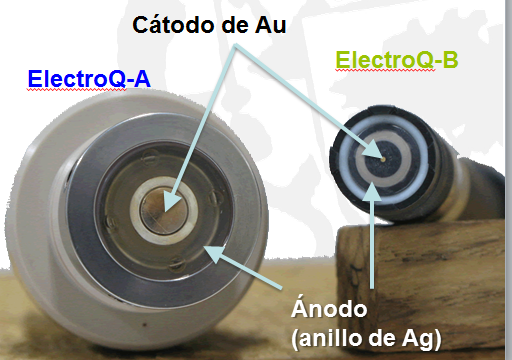
Los sistemas electroquímicos están en su mayoría basados en la celda de Clark con pequeñas variaciones propias de su aplicación y con diferentes soluciones dependiendo de la empresa que lo construye. El electrodo tipo Clark está formado por un cátodo y un ánodo sumergidos en un electrolito. Cuando el oxígeno entra en el sensor a través de una membrana permeable por difusión, se reduce en el cátodo y crea una corriente eléctrica medible y linealmente proporcional a la concentración de oxígeno disuelto.
Los sistemas optoluminiscentes están basados en un optodo, que es la versión óptica del electrodo y utilizan la capacidad de algunos materiales para ver emitir luz a diferente longitud de onda de la que reciben siempre que se encuentren en presencia de moléculas libres de oxígeno, fenómeno llamado amortiguación dinámica de la fluorescencia. Generalmente constan de polímero en el que se deposita la sustancia sensora que estará en contacto con el fluido a medir. Este sensor está unido al emisor de luz por una fibra óptica que a su vez devuelve la luz emitida a diferente longitud de onda al receptor. La relación no es lineal entre la variación de la luz emitida-recibida y la concentración del analito, en nuestro caso oxígeno, sino que sigue la relación de Stern-Volmer. A diferencia del electrodo de Clark, la señal es mayor cuanto menor es la concentración de OD. La variación de la luz emitida reflejada se ha considerado tanto por medida de la variación en la intensidad como por la medida en el desfase de la señal, adoptando hoy en día la mayoría de los fabricantes esta última opción al no depender del tamaño de la muestra ni siquiera de las posibles fluctuaciones de la señal o de pérdida de color del propio sensor. De esta forma, la principal diferencia entre ambas tecnologías es que la electroquímica necesita consumir oxígeno para dar una señal eléctrica proporcional a la presión parcial de oxígeno en el fluido, mientras que la tecnología luminiscente no altera el contenido en oxígeno de la muestra. Así pues, para realizar medidas con el sistema basado en la celda electroquímica es necesario medir el fluido en movimiento, lo cual en muchas operaciones no supone más que incluir el sistema de medida en la línea de proceso, mientras que en otras operaciones se hace necesario implementar este flujo de forma expresa mediante un dispositivo externo (microoxigenación, barricas, estabilización por estabulación….) y puede suponer una fuente de contaminación con el oxígeno atmosférico.
Otra diferencia importante es que el sistema electroquímico ofrece mayor señal eléctrica con mayor contenido en oxígeno disuelto mientras que el principio luminiscente es justamente al revés, la mayor señal se produce cuando menor sea el nivel en OD.
Además de estas diferencias existen otras que afectan lo suficiente como para decantarse en determinadas operaciones por una tecnología. El sistema electroquímico se sirve de una membrana para permear el OD desde el fluido hacia la celda de Clark que en función de la aplicación puede ser un material diferente, pero en todas ellas sufre de problemas de ensuciamiento que requieren de su sustitución de forma periódica, además de necesitar de un periodo de tiempo para que se equilibre el nivel de OD entre el fluido medido y el electrolito dentro del sensor, algo que está en continua variación al ser el oxígeno consumido, en resumen se necesita un tiempo de polarización de la membrana, así como para que se alcance el equilibrio necesario para medir de forma estable el contenido en OD. Estos aspectos suponen un hándicap a la hora de usar este sistema como equipo móvil para realizar medidas sucesivas en diferentes puntos a lo largo de la bodega. Frente a estas particularidades, el sistema luminiscente ofrece soluciones muy interesantes (fig. 3).


La más relevante es la capacidad de situar la sustancia sensora, el luminóforo, en emplazamientos fijos dentro del líquido a medir sin tener que disponer de un equipo, ni siquiera sonda en cada punto. Simplemente se coloca el sensor (conocido como spot o dot ) en una superficie transparente en contacto directo y continuo con el fluido a controlar. Esto implica que este se encuentra equilibrado y posibilita una medida instantánea del OD en ese punto. Además también están disponibles todo tipo de sondas de inmersión ya que estas no son más que fibras ópticas con diferentes configuraciones que disponen de la sustancia sensora luminiscente depositada en el extremo. De esta forma, con un equipo portátil se pueden realizar medidas en todos los puntos de control, ya sean estáticos en depósito, o en tuberías de proceso (trasiegos, movimiento de la vendimia, operaciones de embotellado, estabilización…).
Ahora que están claras tanto las dos necesidades en cuanto a nivel de detección, como las dos tecnologías disponibles en el mercado pasemos a hablar de cómo se comportan ante situaciones concretas. Ante la perspectiva de utilizar un sistema de medida de oxígeno en una bodega hay que tener muy claro qué se quiere controlar y si el parámetro OD nos va a ayudar a tomar decisiones o simplemente va a ser un aparato más a adquirir para seguir la moda. Una vez decididas las operaciones a controlar ya sabremos qué nivel de medida necesitamos, para lo cual nos podremos guiar por los valores descritos por diferentes autores sirviendo los de la figura 1 como referencia.
Ahora hay que tener bien claro que si queremos monitorizar operaciones que disponen de niveles de OD en ppm, estos sistemas no sirven para la medida de niveles inferiores de ppb. Aunque sea una cuestión evidente, pues ya se puede saber por las especificaciones técnicas de cada sistema, no siempre se les presta la atención suficiente o bien nos dejamos seducir por un precio mucho más ventajoso que nos hace pensar que bien pueden valer para una necesidad puntual. Esto no quiere decir que no midan sino que las medidas que ofrecen no tienen garantías suficientes. Veamos algunos ejemplos.
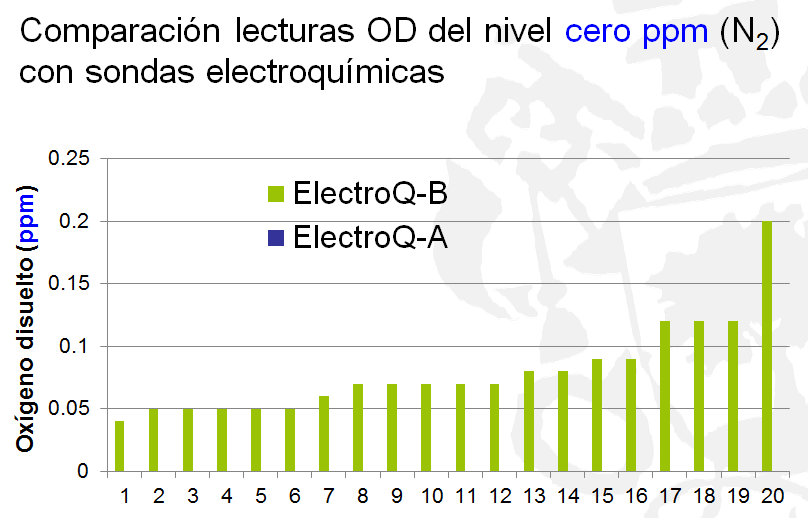
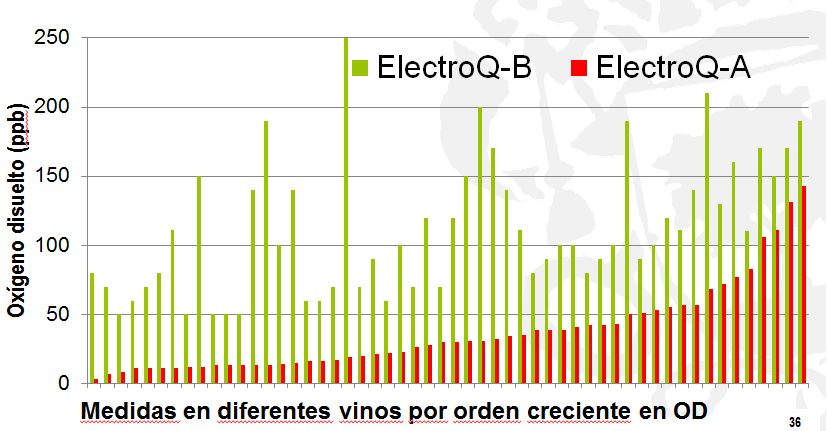
Los sistemas electroquímicos generalmente se calibran con el aire o con dos puntos de calibración (0% con nitrógeno y 100% al aire). En medidas realizadas con dos sensores electroquímicos disponibles en el mercado en nitrógeno (figs. 4 y 5) se aprecia cómo los sistemas de baja resolución (medidas en ppm) nos dan medidas peregrinas en el cero, mientras que en el caso de medidas en vinos con bajos niveles de OD la fiabilidad en la medida del OD es totalmente cuestionable (fig. 6).
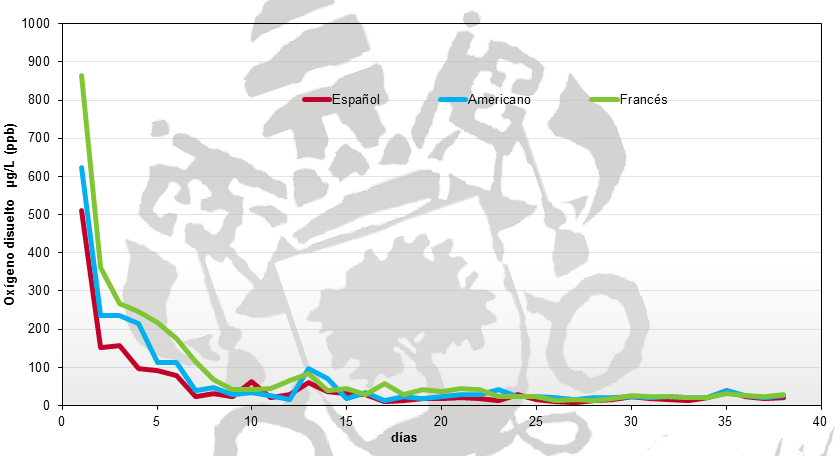
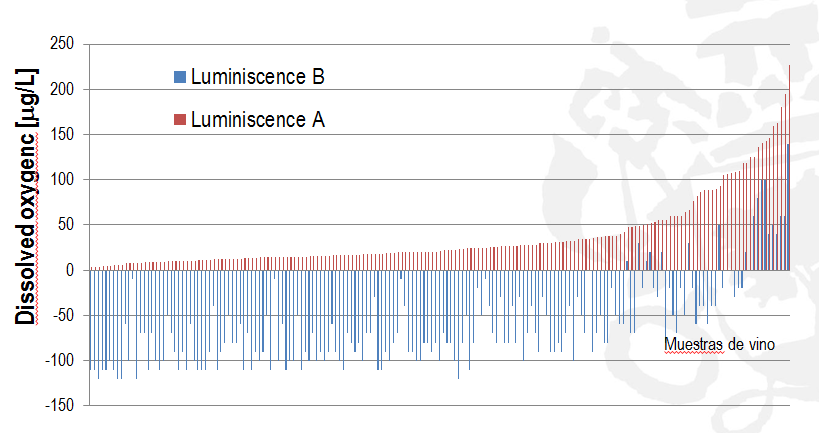
En el caso de los sistemas optoluminiscentes también existen en el mercado diferentes equipos enfocados a las medidas generales y a las medidas de precisión. En este caso ocurre exactamente lo mismo. En medidas realizadas en vinos con niveles de OD bajos, correspondientes a vinos almacenados, en proceso de crianza en barrica o microoxigenados para un tratamiento con alternativos de roble, se ha encontrado que el equipo Luminiscente A ofrecía medidas razonables, mientras que el equipo Luminiscente B ofrecía medidas erráticas, que nuevamente no son útiles y pueden llevarnos a una toma de decisión equivocada (fig. 7).
Esperamos que este análisis sirva para clarificar la situación y os permita analizar la posibilidad de utilizar la medida del OD como un parámetro útil para controlar los procesos de bodega y así decidir en función del momento a controlar si es rentable la compra de un equipo de baja resolución, o incurrir en un gasto en torno a diez veces mayor para comprar un equipo que os permita medir bajos niveles de OD con las garantías suficientes.
Agradecimientos
Los autores agradecen la financiación de la Junta de Castilla y León (proyecto referencia VA086A11-2) y del Ministerio de Ciencia e Innovación (Proyecto referencia AGL2011-26931).
Bibliografía
1. Vidal, J.C., J.C. Boulet, M. Moutounet. «Les apports d’oxygène au cours des traitements des vins. Bilan des observations sur site. 3ème partie». Revue Française d’Oenologie 2004; 205: 25-33.
2. Vidal, J.C., J.C. Boulet, M. Moutounet. «Les apports d’oxygène au cours des traitements des vins. Bilan des observations sur site. 2ème partie». Revue Française d’Oenologie 2003; 201: 32-34, 36-8.
3. Vidal, J.C. et al. «Les apports d’oxygène au cours des traitements des vins. Bilan des observations sur site. 1ère partie». Revue Française d’Oenologie 2001; 190: 24-31.
4. Castellari, M. et al. «Effects of different enological treatments on dissolved oxygen in wines». Italian Journal of Food Science 2004; 16 (3): 387-96.
5. Pénicaud, C. et al. «Oxygen quantification methods and application to the determination of oxygen diffusion and solubility coefficients in food». Food Reviews International 2011; 28 (2): 113-45.
6. Kautsky H. «Quenching of luminescence by oxygen». Transactions of the Faraday Society 1939; 35: 216-9.